ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
โรคกู๊ดพาสเจอร์: สาเหตุ อาการ การวินิจฉัย การรักษา
ตรวจสอบล่าสุด: 12.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
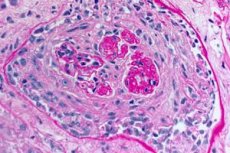
กลุ่มอาการ Goodpasture เป็นกลุ่มอาการที่เกิดจากภูมิคุ้มกันทำลายตนเองซึ่งเกี่ยวข้องกับเลือดออกในถุงลม ปอด และไตอักเสบที่เกิดจากแอนติบอดีต่อต้าน GBM ที่ไหลเวียนอยู่ กลุ่มอาการ Goodpasture มักเกิดขึ้นในบุคคลที่มีแนวโน้มทางพันธุกรรมที่สูบบุหรี่ แต่การสูดดมไฮโดรคาร์บอนและการติดเชื้อไวรัสในทางเดินหายใจก็เป็นปัจจัยเพิ่มเติมได้เช่นกัน อาการของโรค Goodpasture ได้แก่ หายใจลำบาก ไอ อ่อนเพลีย ไอเป็นเลือด และ/หรือปัสสาวะเป็นเลือด กลุ่มอาการ Goodpasture มักสงสัยในผู้ป่วยที่ไอเป็นเลือดหรือปัสสาวะเป็นเลือด และได้รับการยืนยันจากการมีแอนติบอดีต่อต้าน GBM ในเลือด การรักษาโรค Goodpasture ได้แก่ การแลกเปลี่ยนพลาสมา กลูโคคอร์ติคอยด์ และยากดภูมิคุ้มกัน เช่น ไซโคลฟอสฟามายด์ การพยากรณ์โรคจะดีหากเริ่มการรักษาก่อนที่จะเกิดภาวะระบบทางเดินหายใจหรือไตวาย
โรค Goodpasture's syndrome ได้รับการอธิบายครั้งแรกโดย Goodpasture ในปี 1919 โรค Goodpasture's syndrome เป็นโรคที่เกิดจากการรวมกันของภาวะไตอักเสบและเลือดออกในถุงลมปอดโดยมีแอนติบอดีต่อ GBM โรค Goodpasture's syndrome มักแสดงอาการเป็นการรวมกันของภาวะเลือดออกในถุงลมปอดและไตอักเสบ แต่บางครั้งก็ทำให้เกิดภาวะไตอักเสบเพียงแห่งเดียว (10-20%) หรือปอดได้รับผลกระทบ (10%) ผู้ชายได้รับผลกระทบมากกว่าผู้หญิง
อะไรที่ทำให้เกิดโรค Goodpasture?
สาเหตุของโรคยังไม่ชัดเจน สันนิษฐานว่ามีแนวโน้มทางพันธุกรรมที่จะเป็นโรค Goodpasture's syndrome โดยเครื่องหมายของโรคนี้ถือว่าเกิดจากการมี HLA-DRW2 นอกจากนี้ ยังมีมุมมองเกี่ยวกับบทบาทที่เป็นไปได้ของการติดเชื้อไวรัสก่อนหน้านี้ (ไวรัสตับอักเสบเอและโรคไวรัสอื่นๆ) อันตรายจากอุตสาหกรรม และยา (โดยเฉพาะ D-penicillamine)
พื้นฐานของพยาธิสภาพของโรค Goodpasture คือการสร้างแอนติบอดีต่อเยื่อฐานของหลอดเลือดฝอยที่ไตและถุงลม แอนติบอดีเหล่านี้จัดอยู่ในกลุ่ม IgG โดยจะจับกับแอนติบอดีของเยื่อฐานเมื่อมีส่วนประกอบ C3 ของคอมพลีเมนต์ ส่งผลให้เกิดการอักเสบของภูมิคุ้มกันในไตและถุงลมปอดในเวลาต่อมา
แอนติบอดีต่อต้าน GBM มุ่งเป้าไปที่โดเมนที่ไม่ใช่คอลลาเจน (NC-1) ของคอลลาเจนประเภท IV 3 สาย ซึ่งพบในความเข้มข้นสูงสุดในเยื่อฐานของหลอดเลือดฝอยไตและปอด การสัมผัสกับปัจจัยด้านสิ่งแวดล้อม เช่น การสูบบุหรี่ การติดเชื้อไวรัสทางเดินหายใจเฉียบพลัน และการสูดดมสารแขวนลอยไฮโดรคาร์บอเนต (บ่อยครั้งกว่า) และปอดบวมซึ่งเกิดขึ้นน้อยกว่า จะทำให้แอนติเจนของหลอดเลือดฝอยถุงลมแสดงต่อแอนติบอดีที่หมุนเวียนในผู้ที่มีแนวโน้มทางพันธุกรรม (ส่วนใหญ่มักเป็นพาหะของอัลลีล HLA-DRwl5, -DR4 และ -DRB1) แอนติบอดีต่อต้าน GBM ที่หมุนเวียนจะจับกับเยื่อฐาน ตรึงคอมพลีเมนต์ และกระตุ้นให้เกิดการอักเสบของเซลล์ ส่งผลให้เกิดโรคไตอักเสบและ/หรือหลอดเลือดฝอยปอดอักเสบ
อาจมีออโตแอนติเจนของเยื่อฐานของหลอดเลือดฝอยของไตและถุงลมที่เหมือนกัน ออโตแอนติเจนเกิดขึ้นจากอิทธิพลของปัจจัยก่อโรค ปัจจัยก่อโรคที่ไม่ทราบแน่ชัดจะทำลายและปรับเปลี่ยนโครงสร้างของเยื่อฐานของไตและปอด การขับถ่ายผลิตภัณฑ์ที่ย่อยสลายได้ของเยื่อฐานของไตจะช้าลงและลดลงเมื่อได้รับความเสียหาย ซึ่งเป็นปัจจัยพื้นฐานที่ก่อให้เกิดความเสียหายต่อไตและปอดจากภูมิคุ้มกันทำลายตนเองโดยธรรมชาติ ยังคงไม่ทราบแน่ชัดว่าส่วนประกอบใดของเยื่อฐานที่กลายเป็นออโตแอนติเจน ปัจจุบันสันนิษฐานว่านี่คือส่วนประกอบโครงสร้างภายในของเยื่อฐานของไต ซึ่งก็คือคอลลาเจนชนิดที่ 4 ที่เรียกว่าโซ่ A3
คอมเพล็กซ์ภูมิคุ้มกันที่เกิดขึ้นจะสะสมอยู่ตามเยื่อฐานของหลอดเลือดฝอยในไต ซึ่งนำไปสู่การพัฒนาของกระบวนการอักเสบของภูมิคุ้มกันในไตของโกลเมอรูลัส (glomerulonephritis) และถุงลม (alveolitis) เซลล์หลักที่เกี่ยวข้องกับการพัฒนาของการอักเสบของภูมิคุ้มกันนี้ ได้แก่ เซลล์ทีลิมโฟไซต์ โมโนไซต์ เอนโดทีลิโอไซต์ เม็ดเลือดขาวพหุรูปนิวเคลียส แมคโครฟาจของถุงลม ปฏิสัมพันธ์ระหว่างเซลล์เหล่านี้เกิดขึ้นจากตัวกลางโมเลกุล ไซโตไคน์ (ปัจจัยการเจริญเติบโต - เกล็ดเลือด อินซูลินไลค์ การแปลงบี อินเตอร์ลิวคิน-1 ปัจจัยเนโครซิสของเนื้องอก ฯลฯ) เมแทบอไลต์ของกรดอะราคิโดนิก อนุมูลอิสระออกซิเจน เอนไซม์โปรตีโอไลติก โมเลกุลยึดเกาะมีบทบาทสำคัญในการพัฒนาของการอักเสบของภูมิคุ้มกัน
การกระตุ้นแมคโครฟาจในถุงลมมีความสำคัญอย่างยิ่งต่อการพัฒนาของโรคถุงลมโป่งพองในกลุ่มอาการ Goodpasture เมื่อกระตุ้นแล้ว แมคโครฟาจจะหลั่งไซโตไคน์ประมาณ 40 ชนิด ไซโตไคน์กลุ่ม I (เคโมแท็กซิน ลิวโคไตรอีน อินเตอร์ลิวคิน-8) ช่วยเพิ่มการไหลของเม็ดเลือดขาวที่มีนิวเคลียสจำนวนมากเข้าสู่ปอด ไซโตไคน์กลุ่ม II (ปัจจัยการเจริญเติบโต - เกล็ดเลือด แมคโครฟาจ) ส่งเสริมการเคลื่อนที่ของไฟโบรบลาสต์เข้าสู่ปอด นอกจากนี้ แมคโครฟาจในถุงลมยังผลิตออกซิเจนรูปแบบที่ออกฤทธิ์ ซึ่งก็คือโปรตีเอส ซึ่งสามารถทำลายเนื้อเยื่อปอดได้
พยาธิสภาพของโรคกู๊ดพาสเจอร์
อาการทางพยาธิวิทยาหลักๆ ของโรค Goodpasture ได้แก่:
- ความเสียหายที่เกิดขึ้นกับระบบไหลเวียนเลือดในไตและปอดส่วนใหญ่ ในปอดจะพบภาพของโรคหลอดเลือดดำอักเสบ หลอดเลือดแดงอักเสบ หลอดเลือดฝอยอักเสบ ซึ่งมีอาการรุนแรงและขยายตัวอย่างรวดเร็ว ความเสียหายของหลอดเลือดฝอยพบได้มากในบริเวณผนังระหว่างถุงลม ถุงลมอักเสบโดยมีเลือดออกในถุงลม ความเสียหายของไตมีลักษณะเฉพาะคือมีการพัฒนาของโรคไตอักเสบจากการขยายพันธุ์นอกเส้นเลือดฝอย ส่งผลให้เกิดภาวะไฮยาลินและพังผืดตามมา ซึ่งนำไปสู่ภาวะไตวาย
- มีเลือดออกภายในถุงลมอย่างชัดเจน
- การพัฒนาของโรค hemosiderosis ในปอดและโรค pneumosclerosis ในระดับความรุนแรงที่แตกต่างกัน อันเป็นผลจากการเกิดโรคถุงลมอักเสบ
อาการของโรคกู๊ดพาสเจอร์
โรคนี้มักแสดงอาการทางคลินิกของโรคปอด อาการที่เด่นชัดที่สุดคืออาการไอเป็นเลือด อย่างไรก็ตาม อาการไอเป็นเลือดอาจไม่ปรากฏหากมีอาการเลือดออก และผู้ป่วยอาจมีอาการแทรกซ้อนจากการเอ็กซ์เรย์ทรวงอก หรือมีอาการแทรกซ้อนและหายใจลำบากหรือล้มเหลว อาการหายใจลำบาก (ส่วนใหญ่มักเกิดขึ้นเมื่อออกแรง) ไอ อ่อนเพลีย ทำงานได้ลดลง เจ็บหน้าอก มีไข้ และน้ำหนักลด ผู้ป่วยสูงสุด 40% มีภาวะเลือดออกในปัสสาวะ แม้ว่าเลือดออกในปอดอาจมาก่อนอาการทางไตได้หลายสัปดาห์หรือหลายปี
ในระหว่างที่ไอเป็นเลือด อาจทำให้หายใจลำบากมากขึ้น อาการอ่อนแรงและความสามารถในการทำงานลดลงก็เป็นปัญหาเช่นกัน
อาการของโรค Goodpasture จะแตกต่างกันไปในแต่ละช่วงเวลา ตั้งแต่ปอดใสเมื่อฟังเสียงปอด ไปจนถึงเสียงปอดแตกและแห้ง ผู้ป่วยบางรายมีอาการบวมน้ำรอบนอกและซีดเนื่องจากโรคโลหิตจาง
ระหว่างการตรวจร่างกาย ผู้ป่วยจะสังเกตอาการผิวซีด เยื่อเมือกเขียวคล้ำ ใบหน้าบวมหรือบวมมาก ความแข็งแรงของกล้ามเนื้อลดลง และน้ำหนักลด อุณหภูมิร่างกายมักจะสูงขึ้นจนมีไข้
เมื่อทำการเคาะปอด อาจพบว่าเสียงเคาะสั้นลงในบริเวณที่มีเลือดออกในปอดอย่างกว้างขวาง แต่พบได้น้อยครั้ง โดยส่วนใหญ่แล้วจะไม่มีการเปลี่ยนแปลงของเสียงเคาะ
อาการฟังเสียงที่เป็นลักษณะเฉพาะของโรค Goodpasture คือ หายใจมีเสียงหวีดทั้งแบบแห้งและแบบมีเสียงหวีด โดยจำนวนครั้งของเสียงหวีดจะเพิ่มขึ้นอย่างมีนัยสำคัญในระหว่างหรือหลังอาการไอเป็นเลือด
เมื่อตรวจระบบหัวใจและหลอดเลือด จะพบว่ามีความดันโลหิตสูงขึ้น อาจมีอาการหัวใจเต้นช้าไปทางซ้าย เสียงหัวใจเบาลง เสียงหัวใจบีบตัวผิดปกติแบบเบา และเสียงเยื่อหุ้มหัวใจเสียดสีปรากฏขึ้นพร้อมกับอาการไตวายรุนแรง หากไตได้รับความเสียหายมากขึ้นเรื่อยๆ โดยมีสาเหตุมาจากความดันโลหิตสูงขึ้นอย่างรุนแรง อาจเกิดภาวะหัวใจห้องล่างซ้ายล้มเหลวเฉียบพลันร่วมกับอาการหอบหืดและอาการบวมน้ำในปอดได้ โดยปกติแล้ว ภาวะนี้จะเกิดขึ้นในระยะสุดท้ายของโรค
โดยทั่วไป ความเสียหายของไตจะแสดงออกมาในภายหลัง หลังจากระยะเวลาหนึ่งหลังจากการพัฒนาของอาการทางปอด อาการทางคลินิกเฉพาะของโรคไต ได้แก่ เลือดออกในปัสสาวะ (บางครั้งเป็นเลือดในปัสสาวะมาก) ไตวายที่ดำเนินไปอย่างรวดเร็ว ปัสสาวะน้อย ความดันโลหิตสูง
ใน 10-15% ของกรณี อาการ Goodpasture จะเริ่มด้วยอาการทางคลินิกของพยาธิวิทยาของไต โดยมีอาการทางคลินิกของโรคไตอักเสบ (ปัสสาวะน้อย บวม ความดันโลหิตสูง ซีดมาก) จากนั้นอาการของปอดเสียหายจะตามมา ผู้ป่วยหลายรายอาจมีอาการปวดกล้ามเนื้อและปวดข้อ
ไม่ว่าจะมีรูปแบบใดที่เริ่มต้นขึ้นก็ตาม ในกรณีส่วนใหญ่ โรค Goodpasture มักจะรุนแรง โรคจะค่อยๆ ดำเนินไป ปอดและไตวายรุนแรงจะค่อยๆ พัฒนาไป อายุขัยของผู้ป่วยนับตั้งแต่เริ่มเป็นโรคจะอยู่ระหว่างหลายเดือนถึง 1-3 ปี ส่วนใหญ่ผู้ป่วยจะเสียชีวิตจากภาวะยูรีเมียหรือเลือดออกในปอด
สิ่งที่รบกวนคุณ?
การวินิจฉัยโรค Goodpasture
การวินิจฉัยโรค Goodpasture syndrome จำเป็นต้องตรวจหาแอนติบอดีต่อ GBM ในซีรั่มด้วยวิธี indirect immunofluorescence หรือหากทำได้ ให้ใช้ direct enzyme-linked immunosorbent assay (ELISA) ร่วมกับ recombinant human NC-1 a3 การทดสอบทางซีรั่มอื่นๆ เช่น การทดสอบ antinuclear antibody (ANA) ใช้เพื่อตรวจหา SLE และ antistreptolysin-O titer เพื่อตรวจหา glomerulonephritis หลังการติดเชื้อสเตรปโตค็อกคัส ซึ่งอาจเป็นสาเหตุของโรคปอดและไตอักเสบหลายกรณี ผล ANCA เป็นบวก (ในตัวอย่างจากส่วนปลาย) ใน 25% ของผู้ป่วยโรค Goodpasture syndrome อาจต้องตัดชิ้นเนื้อไตหากมีภาวะ glomerulonephritis (เลือดออกในปัสสาวะ โปรตีนในปัสสาวะ ตะกอนเม็ดเลือดแดงจากการตรวจปัสสาวะ และ/หรือไตวาย) โรคไตอักเสบแบบเนื้อตายเป็นบางส่วนแบบลุกลามอย่างรวดเร็วและดำเนินไปอย่างค่อยเป็นค่อยไปพบได้จากการตรวจชิ้นเนื้อในผู้ป่วยโรค Goodpasture และจากสาเหตุอื่นๆ ของโรคไตในปอด การย้อมอิมมูโนฟลูออเรสเซนซ์ของเนื้อเยื่อไตหรือปอดโดยทั่วไปจะเผยให้เห็นการสะสมเชิงเส้นของ IgG ตามเส้นเลือดฝอยของไตหรือถุงลม นอกจากนี้ยังพบในไตของผู้ป่วยเบาหวานและโรคไตอักเสบแบบมีลิ่ม ซึ่งเป็นโรคที่พบได้น้อยที่ทำให้เกิดโรคไตในปอดแต่การตรวจหาแอนติบอดี GBM ในโรคเหล่านี้ไม่จำเพาะ
การทดสอบการทำงานของปอดและการล้างหลอดลมและถุงลมไม่ใช่การวินิจฉัยโรค Goodpasture แต่สามารถใช้ยืนยันการมีอยู่ของเลือดออกในถุงลมทั่วร่างกายในผู้ป่วยที่เป็นโรคไตอักเสบและมีการแทรกซึมของเลือดในปอดแต่ไม่มีเลือดไหล การล้างของเหลวที่ยังคงมีเลือดออกหลังจากการล้างหลายครั้งอาจยืนยันโรคเลือดออกทั่วร่างกายได้ โดยเฉพาะหากมีการลดลงพร้อมกันของค่าฮีมาโตคริต
 [ 3 ]
[ 3 ]
การวินิจฉัยทางห้องปฏิบัติการของโรค Goodpasture
- การตรวจเลือดทั่วไป ลักษณะเด่น ได้แก่ ภาวะโลหิต จางจากการขาดธาตุเหล็ก ภาวะสีซีด ภาวะสีซีด ภาวะเม็ดเลือดแดงไม่เต็ม ภาวะเม็ดเลือดแดงมีสีจางมาก นอกจากนี้ยังพบเม็ดเลือดขาวสูง การเคลื่อนตัวไปทางซ้ายของสูตรเม็ดเลือดขาว และค่า ESR เพิ่มขึ้นอย่างมีนัยสำคัญ
- การวิเคราะห์ปัสสาวะโดยทั่วไปพบโปรตีนในปัสสาวะ (ระดับโปรตีนในปัสสาวะอาจมีความสำคัญ) ทรงกระบอก (เม็ด ใส เม็ดเลือดแดง) เม็ดเลือดแดง (อาจเกิดภาวะเลือดออกในปัสสาวะ) เมื่อภาวะไตวายเรื้อรังดำเนินไป ความหนาแน่นสัมพัทธ์ของปัสสาวะจะลดลง และเกิดภาวะปัสสาวะไม่สุดในการทดสอบ Zimnitsky
- การตรวจเลือดทางชีวเคมี ระดับยู เรี ยครีเอตินินแฮปโตโกลบิน ซีโรมูคอยด์ เอ2 และแกมมาโกลบูลิน ในเลือดเพิ่มขึ้น ปริมาณธาตุเหล็ก ลดลง
- การศึกษาทางภูมิคุ้มกัน อาจตรวจพบการลดลงของจำนวนเซลล์ทีลิมโฟไซต์ที่กดภูมิคุ้มกัน โดยตรวจพบ คอมเพล็กซ์ภูมิคุ้มกันที่ไหลเวียนตรวจหาแอนติบอดีต่อเยื่อฐานของหลอดเลือดฝอยไตและถุงลมด้วยวิธีอิมมูโนฟลูออเรสเซนซ์ทางอ้อมหรือวิธีเรดิโออิมมูโนโลยี
- การตรวจเสมหะพบว่าเสมหะมีเม็ดเลือดแดงจำนวนมาก ตรวจพบเฮโมไซเดอริน ไซเดอโรฟาจ
การวินิจฉัยด้วยเครื่องมือของโรค Goodpasture
- การตรวจเอกซเรย์ปอด อาการเอกซเรย์ที่เด่นชัดคือ ปอดมีการแพร่กระจายของเนื้องอกในปอดที่บริเวณรากปอดไปยังส่วนล่างและส่วนกลางของปอด รวมถึงเนื้องอกคล้ายเมฆที่ค่อยๆ แพร่กระจายแบบสมมาตรทั้งสองข้าง
- การศึกษาการทำงานของการหายใจภายนอก การตรวจสมรรถภาพปอดจะเผยให้เห็นภาวะหายใจล้มเหลวแบบจำกัด (ความสามารถในการหายใจลดลง) เมื่อโรคดำเนินไป ภาวะหายใจล้มเหลวแบบอุดกั้นก็จะตามมาด้วย (ค่า FEV1 ลดลง ดัชนี Tiffeneau)
- ECG แสดงอาการกล้ามเนื้อหัวใจเสื่อมอย่างรุนแรงจากภาวะโลหิตจางและภาวะขาดออกซิเจน (การลดลงของแอมพลิจูดของคลื่น T และช่วง ST ในลีดจำนวนมาก โดยส่วนใหญ่มักอยู่ในลีดของทรวงอกด้านซ้าย) ภาวะความดันโลหิตสูงอย่างรุนแรงอาจแสดงอาการกล้ามเนื้อหัวใจห้องล่างซ้ายโต
- การวิเคราะห์ก๊าซในเลือดเผยให้เห็นภาวะเลือดแดงขาดออกซิเจน
- การตรวจชิ้นเนื้อปอดและไต จะทำการตรวจชิ้นเนื้อปอด (การตรวจชิ้นเนื้อแบบเปิด) และไตเพื่อยืนยันการวินิจฉัยขั้นสุดท้าย หากไม่สามารถวินิจฉัยโรคได้อย่างแม่นยำด้วยวิธีการที่ไม่รุกราน จะทำการตรวจชิ้นเนื้อทางเนื้อเยื่อวิทยาและภูมิคุ้มกัน อาการต่อไปนี้เป็นลักษณะเฉพาะของโรคกูดพาสเจอร์:
- การมีสัญญาณทางสัณฐานวิทยาของโรคไตอักเสบ (glomerulonephritis) (ส่วนมากมักเป็นโรคที่นอกเส้นเลือดฝอย) โรคถุงลมอักเสบมีเลือดออก โรคฮีโมไซเดอโรซิส และโรคพังผืดในเนื้อเยื่อระหว่างช่องว่าง
- การตรวจหาการสะสมเชิงเส้นของ IgG และส่วนประกอบเสริม C3บนเยื่อฐานของถุงลมปอดและกลุ่มไตโดยใช้วิธีอิมมูโนฟลูออเรสเซนซ์
เกณฑ์การวินิจฉัยโรคกู๊ดพาสเจอร์
ในการวินิจฉัยโรค Goodpasture ควรใช้เกณฑ์ดังต่อไปนี้
- การรวมกันของพยาธิสภาพของปอดและพยาธิสภาพของไต เช่น ไอเป็นเลือด (มักมีเลือดออกในปอด) หายใจถี่ และอาการของโรคไตอักเสบ
- โรคมีการดำเนินไปอย่างต่อเนื่องและมีอาการระบบทางเดินหายใจและไตวายตามมา
- การเกิดโรคโลหิตจางจากการขาดธาตุเหล็ก
- การตรวจจับระหว่างการตรวจเอกซเรย์ปอดของการแทรกซึมคล้ายเมฆสองข้างจำนวนหลายจุดโดยมีพื้นหลังเป็นความผิดปกติของรูปแบบตาข่ายของปอด
- การตรวจหาค่าไทเตอร์สูงของแอนติบอดีที่ไหลเวียนไปยังเยื่อฐานของไตและถุงลม
- การตรวจหาการสะสมเชิงเส้นของ IgG และส่วนประกอบเสริม C3 บนเยื่อฐานของหลอดเลือดฝอยของไตและถุงลม
- ไม่มีอาการทางระบบอื่น ๆ (ยกเว้นทางปอดและไต)
การวินิจฉัยแยกโรค Goodpasture
โรค Goodpasture ต้องแยกความแตกต่างจากโรคหลายชนิดที่แสดงอาการเป็นเลือดหรือเลือดออกในปอด จำเป็นต้องแยกโรคเนื้องอกของหลอดลมและปอด วัณโรค ฝีในปอด หลอดลมโป่งพอง โรคหัวใจและหลอดเลือด (ทำให้เกิดการคั่งของเลือดและความดันโลหิตสูงในระบบไหลเวียนเลือดในปอด) หลอดเลือดอักเสบทั่วร่างกาย เลือดออกในปอด
โครงการตรวจคัดกรองโรค Goodpasture
- การตรวจเลือดและปัสสาวะทั่วไป
- การตรวจเลือดทางชีวเคมี: การกำหนดโปรตีนทั้งหมดและเศษส่วนของโปรตีน ครีเอตินินและยูเรีย ทรานส์อะมิเนส ซีโรมูคอยด์ แฮปโตโกลบิน ไฟบริน เหล็ก
- การตรวจเสมหะ: การตรวจเซลล์วิทยา การตรวจหาไซเดอโรฟาจ
- การศึกษาทางภูมิคุ้มกัน: การกำหนดปริมาณของเซลล์บีและทีลิมโฟไซต์ กลุ่มย่อยของเซลล์ที อิมมูโนโกลบูลิน คอมเพล็กซ์ภูมิคุ้มกันที่ไหลเวียน แอนติบอดีต่อเยื่อฐานของไตและถุงลม
- การตรวจเอกซเรย์ปอด
- คลื่นไฟฟ้าหัวใจ
- การตรวจสมรรถภาพปอด
- การตรวจชิ้นเนื้อปอดและไต
ต้องการทดสอบอะไรบ้าง?
การรักษาอาการโรคกู๊ดพาสเจอร์
การรักษาโรค Goodpasture syndrome ได้แก่ การแลกเปลี่ยนพลาสมาทุกวันหรือทุกๆ วันเว้นวันเป็นเวลา 2 ถึง 3 สัปดาห์ (การแลกเปลี่ยนพลาสมา 4 ลิตร) เพื่อกำจัดแอนติบอดีต่อ GBM ร่วมกับกลูโคคอร์ติคอยด์ทางเส้นเลือด (โดยปกติคือเมทิลเพรดนิโซโลน 1 กรัม นานอย่างน้อย 20 นาทีทุกๆ วันเว้นวัน 3 ครั้ง ร่วมกับเพรดนิโซโลน 1 มก./กก. น้ำหนักตัวต่อวัน) และไซโคลฟอสเฟไมด์ (2 มก./กก. วันละครั้ง) เป็นเวลา 6 ถึง 12 เดือนเพื่อป้องกันการสร้างแอนติบอดีใหม่ อาจลดปริมาณการบำบัดลงเมื่อการทำงานของปอดและไตไม่ดีขึ้น อัตราการเสียชีวิตในระยะยาวเกี่ยวข้องกับระดับความบกพร่องของไตเมื่อเริ่มเป็นโรค ผู้ป่วยที่ต้องฟอกไตในระยะเริ่มต้นและผู้ที่มีเนฟรอนรูปพระจันทร์เสี้ยวมากกว่า 50% จากการตรวจชิ้นเนื้อจะมีอายุขัยน้อยกว่า 2 ปี และมักต้องฟอกไต เว้นแต่จะพิจารณาการปลูกถ่ายไต อาการไอเป็นเลือดอาจเป็นสัญญาณบ่งชี้ที่ดี เนื่องจากทำให้ตรวจพบโรคได้เร็วขึ้น ผู้ป่วยส่วนน้อยที่ตรวจพบ ANCA-positive ตอบสนองต่อการรักษาโรค Goodpasture ได้ดีกว่า ผู้ป่วยบางรายอาจกลับมาเป็นโรคซ้ำได้ และมักเกิดจากการสูบบุหรี่และการติดเชื้อทางเดินหายใจต่อเนื่อง ในผู้ป่วยโรคไตวายเรื้อรังระยะสุดท้ายที่ได้รับการปลูกถ่ายไต โรคอาจกลับมาเป็นโรคซ้ำได้ในบริเวณที่ปลูกถ่าย
โรค Goodpasture syndrome มีแนวโน้มจะเป็นอย่างไร?
โรค Goodpasture มักลุกลามอย่างรวดเร็วและอาจถึงแก่ชีวิตได้ เว้นแต่จะได้รับการวินิจฉัยและรักษาอย่างทันท่วงที การพยากรณ์โรคจะดีหากเริ่มการรักษาก่อนที่จะเกิดภาวะระบบทางเดินหายใจหรือไตวาย
การมีชีวิตรอดทันทีที่เกิดเลือดออกในปอดและภาวะระบบทางเดินหายใจล้มเหลวสัมพันธ์กับการทำให้ทางเดินหายใจเปิดได้ การใส่ท่อช่วยหายใจและใช้เครื่องช่วยหายใจเป็นสิ่งที่แนะนำสำหรับผู้ป่วยที่มีระดับก๊าซในเลือดแดงอยู่ในระดับที่ไม่แน่นอนและมีแนวโน้มจะเกิดภาวะระบบทางเดินหายใจล้มเหลว

