ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
โพลีไมโครไจเรียของสมอง
ตรวจสอบล่าสุด: 12.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
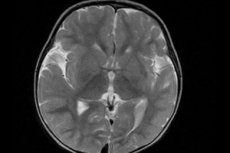
ความผิดปกติแต่กำเนิด – การเกิดการบิดตัวผิดปกติเล็กน้อยหลายครั้งพร้อมกับการเปลี่ยนแปลงทั่วไปในโครงสร้างเซลล์ของเปลือกสมอง – เรียกว่า polymicrogyria ของสมอง (จากภาษาละติน gyrus – การบิดตัว) [ 1 ]
ระบาดวิทยา
ตามสถิติ พบว่าในบรรดาภาวะผิดปกติของสมอง ทุกประเภท ความผิดปกติแต่กำเนิดของคอร์เทกซ์พบได้ประมาณหนึ่งในสามของกรณี แต่ไม่มีข้อมูลเกี่ยวกับความชุกของโพลีไมโครไจเรียแบบแยกเดี่ยว
สาเหตุ โพลีไมโครไจเรีย
ในขณะที่สาเหตุที่เฉพาะเจาะจงของโพลีไมโครไจเรียยังคงอยู่ในระหว่างการศึกษาวิจัย สาระสำคัญของสาเหตุ – เช่นเดียวกับข้อบกพร่องทางพัฒนาการทั้งหมดของสมอง – อยู่ที่ความเบี่ยงเบนของการพัฒนาตัวอ่อน [ 2 ]
ในกรณีนี้ กระบวนการสร้างเกลียวในสมองของทารกในครรภ์จะถูกขัดขวาง โดยการสร้างรอยพับที่มีลักษณะเฉพาะของเปลือกสมอง ซึ่งเริ่มขึ้นในช่วงกลางของการตั้งครรภ์โดยประมาณ รอยพับเหล่านี้ก่อตัวขึ้นจากด้านบนของรอยพับเหล่านี้ และร่องเกิดขึ้นจากรอยบุ๋มระหว่างรอยพับเหล่านี้ ในสภาพที่มีพื้นที่จำกัดในกะโหลกศีรษะ การสร้างรอยพับและร่องจะทำให้พื้นที่ของเปลือกสมองเพิ่มขึ้น [ 3 ]
ความผิดปกติของการพัฒนาของเปลือกสมองในครรภ์ส่วนใหญ่มักเกิดจากความผิดปกติของโครโมโซมและการกลายพันธุ์ของยีน อาจเป็นการกลายพันธุ์ของยีนหนึ่งหรือการลบยีนที่อยู่ติดกันหลายยีน [ 4 ]
โพลีไมโครไจเรียสามารถแยกได้ แต่สามารถเกิดขึ้นได้พร้อมกับความผิดปกติทางสมองอื่น ๆ ด้วยเช่นกัน – กลุ่มอาการที่กำหนดโดยพันธุกรรม โดยเฉพาะอย่างยิ่งกับกลุ่มอาการ DiGeorge (กลุ่มอาการ 22q11.2 โครโมโซมขาดหายไป); [ 5 ] กลุ่มอาการ Adams-Oliver, Zellweger, Walker-Warburg; กลุ่มอาการ Aicardi (มีการสร้างคอร์ปัส คัลโลซัมไม่ขึ้นในสมอง), กลุ่มอาการ Smith-Kingsmore (มีศีรษะโต), กลุ่มอาการ Goldberg-Shprintzen (มีศีรษะเล็กและใบหน้าผิดปกติ) ฯลฯ [ 6 ], [ 7 ]
ปัจจัยเสี่ยง
ผู้เชี่ยวชาญพิจารณาปัจจัยเสี่ยงต่อไปนี้สำหรับการพัฒนาของโรคโพลีไมโครไจเรีย:
- ข้อบกพร่องทางพันธุกรรมที่ถ่ายทอดทางพันธุกรรม;
- การกลายพันธุ์ทางพันธุกรรมโดยธรรมชาติในตัวอ่อน
- ผลกระทบเชิงลบต่อทารกในครรภ์จากสารพิษหรือการติดเชื้อ โดยเฉพาะการติดเชื้อไซโตเมกะโลไวรัสในระหว่างตั้งครรภ์
- ภาวะขาดเลือดในสมองเนื่องจากการไหลเวียนของเลือดไปยังรกไม่เพียงพอและทารกได้รับออกซิเจน ไม่เพียงพอ
- เลือดออกใต้เยื่อหุ้มสมองของทารกในครรภ์จากสาเหตุต่างๆ [ 8 ]
กลไกการเกิดโรค
แม้ว่ากลไกทางสรีรวิทยาที่อยู่เบื้องหลังการเกิดไจเรียจะยังไม่ชัดเจนจนถึงปัจจุบัน (มีรูปแบบต่างๆ อยู่หลายแบบ) แต่การเกิดโรคโพลีไมโครไจเรียมีความเกี่ยวข้องกับความผิดปกติของการสร้างเซลล์ประสาทในโครงสร้างของสมอง รวมถึงการอพยพ การแบ่งตัว และการแพร่กระจายของเซลล์ตัวอ่อนในสันประสาท - นิวโรบลาสต์ เช่นเดียวกับความผิดปกติของการสร้างไจเรียในสมองของทารกในครรภ์ที่กล่าวถึงไปแล้ว
ผลจากความผิดปกติดังกล่าวคือความผิดปกติของเยื่อหุ้มเนื้อเยื่อเกี่ยวพันของสมองได้แก่ เยื่อหุ้มสมองชั้นอ่อน (pia mater) และเยื่อหุ้มสมองชั้นอะแรคนอยด์ (arachnoidea mater) รวมถึงการเปลี่ยนแปลงของความหนาและจำนวนของชั้นต่างๆ การรวมตัวของชั้นโมเลกุลของเนื้อเยื่อที่อยู่ติดกัน การเพิ่มขึ้นของหลอดเลือดในเยื่อหุ้มสมอง ส่งผลให้การไหลเวียนเลือดไปเลี้ยงสมองลดลง (และอาจเกิดเลือดออกเฉพาะที่บริเวณคอร์เทกซ์ชั้นอ่อน อาการบวมของเนื้อขาวที่อยู่ด้านล่าง และการฝ่อของส่วนหนึ่งของคอร์เทกซ์) [ 9 ]
ในกระบวนการสร้างเนื้อเยื่อของเปลือกสมอง เยื่อฐานของเปลือกอ่อนมีบทบาทสำคัญ จากการศึกษาพบว่า โพลิไมโครไจเรียและข้อบกพร่องอื่นๆ ของเปลือกสมองอาจเกี่ยวข้องกับการเจริญเติบโตที่ไม่เสถียรของเยื่อนี้ โดยมีข้อบกพร่องในโปรตีนและส่วนประกอบไกลโคโปรตีน (คอลลาเจนชนิดที่ 4 ไฟโบนิคติน ลามินิน เป็นต้น) ซึ่งนำไปสู่การเปลี่ยนแปลงทางพยาธิวิทยาในโครงสร้างเซลล์ของเปลือกสมอง
ยีนที่มีการเปลี่ยนแปลงที่พบในโพลีไมโครไจเรีย เช่น ยีน GPR56 (หรือ ADGRG1) บนโครโมโซม 16q21 ซึ่งเข้ารหัสโปรตีนจีของเยื่อหุ้มเซลล์ของตัวรับการยึดเกาะเซลล์ – การติดต่อระหว่างเซลล์ที่ควบคุมกระบวนการสร้างรูปร่างของตัวอ่อนและกำหนดรูปแบบเนื้อเยื่อหนึ่งรูปแบบใดที่กำลังก่อตัว การกลายพันธุ์ของยีนนี้เกี่ยวข้องกับการพัฒนาโพลีไมโครไจเรียของสมองส่วนหน้าและข้างเดียว [ 10 ]
อาการ โพลีไมโครไจเรีย
หากโรคโพลีไมโครไจเรียส่งผลต่อสมองด้านใดด้านหนึ่งในเด็ก จะเรียกว่าเป็นข้างเดียว และหากคอร์เทกซ์ของทั้งสองซีกได้รับผลกระทบ ความผิดปกติก็จะเป็นแบบสองข้าง ความผิดปกติของคอร์เทกซ์ในรูปแบบของโรคโพลีไมโครไจเรียจะส่งผลต่อคอร์เทกซ์ด้านข้างหลังเป็นหลัก
สัญญาณแรกๆ และภาพทางคลินิกที่เกิดขึ้นตามกาลเวลาขึ้นอยู่กับว่าบริเวณใดของสมองที่ได้รับผลกระทบจากความผิดปกติ
โพลีไมโครไจเรียแบบโฟกัสข้างเดียวส่งผลต่อบริเวณสมองที่ค่อนข้างเล็ก และส่วนใหญ่มักแพร่กระจายไปยังคอร์เทกซ์หน้าผากหรือคอร์เทกซ์หน้าและข้างขม่อม รวมถึงคอร์เทกซ์รอบซิลเวียน ซึ่งอยู่ใกล้กับร่องซิลเวียน (ด้านข้าง) อาการนี้แสดงออกในรูปของอาการชักอาจไม่มีอาการทางระบบประสาทอื่นๆ
อาการแสดงของ polymicrogyria ทั้งสองข้าง ได้แก่ อาการชักที่เป็นซ้ำ ความล่าช้าในการพัฒนา กล้ามเนื้ออ่อนแรง ตาเหล่ ปัญหาในการกลืน (dysphagia) และการพูด (dysarthria)
ดังนั้น นอกเหนือจากอาการชักที่เกิดขึ้นบ่อยครั้งแล้ว โรคโพลีไมโครไจเรียของสมองส่วนหน้าทั้งสองข้างยังแสดงให้เห็นโดยความล่าช้าในการพัฒนาโดยทั่วไปและทางจิตใจของเด็ก โรคอัมพาตครึ่งล่างแบบเกร็ง (อัมพาตแบบอ่อนแรงของแขนขาส่วนบนและล่าง) อาการอะแท็กเซีย (ความผิดปกติของการประสานงานการเคลื่อนไหว) อาการเดินผิดปกติ (การเดินผิดปกติ) และอาการอะแท็กเซีย (ไม่สามารถยืนได้เลย) และอาการอะบาเซีย (เดินไม่ได้) อีกด้วย
ความผิดปกติของไจเรียในสมองส่วนหน้าและข้าง (frontoparietal polymicrogyria) หรือความผิดปกติของไจเรียในสมองส่วนหน้าและข้าง (bilateral frontoparietal polymicrogyria) มีลักษณะเด่นคือ พัฒนาการล่าช้า ความสามารถในการรับรู้ลดลง (ปานกลางหรือรุนแรง) อาการชัก สายตาไม่ประสานกัน ตาเหล่ อาการอะแท็กเซีย กล้ามเนื้อเกร็ง [ 11 ]
หากมีโรคโพลีไมโครไจเรียบริเวณรอบนอกสมองทั้งสองข้าง อาการต่างๆ (ปรากฏตั้งแต่แรกเกิด ในวัยทารก หรือใกล้อายุ 2 หรือ 3 ขวบ) ที่พบได้บ่อยที่สุด ได้แก่ อาการชักและแขนขาเกร็ง กลืนลำบากและน้ำลายไหล อัมพาตกล้ามเนื้อใบหน้า ลิ้น ขากรรไกร และกล่องเสียงทั้งสองข้างบางส่วน ตลอดจนพัฒนาการล่าช้าทั้งด้านทั่วไปและด้านสติปัญญา
รูปแบบที่รุนแรงที่สุดซึ่งส่งผลต่อสมองทั้งหมดคือโรคโพลีไมโครไจเรียทั่วไปทั้งสองข้าง โรคนี้ทำให้เกิดความบกพร่องทางสติปัญญาอย่างรุนแรง ปัญหาด้านการเคลื่อนไหว และอาการชัก ซึ่งเป็นอาการชักเกร็งกระตุกอย่างต่อเนื่อง ซึ่งยากหรือไม่สามารถควบคุมได้ด้วยยา[ 12 ]
ภาวะแทรกซ้อนและผลกระทบ
ผลที่ตามมาของภาวะโพลีไมโครไจเรีย ได้แก่:
- โรคสมองเสื่อมแบบกล้ามเนื้อกระตุกในรูปแบบของอาการชักรุนแรงของโรคลมบ้าหมูทั่วไป - กลุ่มอาการเวสต์;
- ภาวะบกพร่องทางการเคลื่อนไหวและความบกพร่องทางการพูด
- ความบกพร่องทางสติปัญญาและความบกพร่องทางจิตในระดับต่างๆ ในเด็ก
การวินิจฉัย โพลีไมโครไจเรีย
การวินิจฉัยโรคโพลีไมโครไจเรียของสมองจะพิจารณาจากอาการและผลการตรวจทางระบบประสาท รวมถึงการตรวจทางพันธุกรรมและเทคนิคการถ่ายภาพต่างๆ
ในปัจจุบัน การวินิจฉัยด้วยเครื่องมือที่มีข้อมูลมากที่สุดคือการใช้การถ่ายภาพด้วยคลื่นแม่เหล็กไฟฟ้า (MRI) ของสมอง [ 13 ]
การตรวจคลื่นไฟฟ้าสมองใช้เพื่อประเมินการทำงานของสมอง
การวินิจฉัยที่แตกต่างกัน
การวินิจฉัยแยกโรคจะดำเนินการร่วมกับความผิดปกติแต่กำเนิดอื่นๆ ของสมอง รวมถึง pachygyria, schizencephaly, ความผิดปกติของการทำงานของสมองแบบแบ่งกลุ่มอาการ ตลอดจนโรคลมบ้าหมูแบบทั่วไปและเฉพาะที่ที่ไม่ทราบสาเหตุในเด็ก [ 14 ]
ใครจะติดต่อได้บ้าง?
การรักษา โพลีไมโครไจเรีย
การรักษาความผิดปกติแต่กำเนิดนี้มีเป้าหมายเพื่อขจัดอาการ ดังนั้น จึงใช้ยาต้านโรคลมบ้าหมูเพื่อควบคุมอาการชัก
วิธีการรักษาอื่นๆ: การกายภาพบำบัด, กิจกรรมบำบัด, การบำบัดการพูด
การป้องกัน
เมื่อพิจารณาจากสัดส่วนที่สำคัญของการกลายพันธุ์ของยีนตามธรรมชาติที่นำไปสู่การพัฒนาของความผิดปกติของเปลือกสมอง จึงถือว่าการป้องกันเป็นไปไม่ได้
พยากรณ์
ในกรณีส่วนใหญ่ โพลีไมโครไจเรียมีการพยากรณ์โรคที่ไม่ดี โดยผู้ป่วย 87-94% เป็นโรคลมบ้าหมูที่รักษาไม่หายขาดและมีอาการชักซ้ำๆ เด็กจำนวนมากที่มีความผิดปกติทั้งสองข้างหรือมีรอยโรคมากกว่าครึ่งหนึ่งของอาการชักในซีกใดซีกหนึ่งจะเสียชีวิตในวัยเด็ก

