ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
โรคถุงน้ำในรังไข่หลายใบ
ตรวจสอบล่าสุด: 04.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
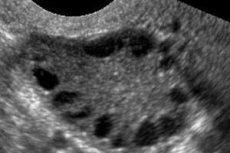
โรคถุงน้ำในรังไข่หลายใบเป็นโรคที่เกิดจากปัจจัยหลายอย่างซึ่งมีลักษณะเฉพาะคือ ความผิดปกติของรอบเดือน การไม่ตกไข่เรื้อรัง ภาวะฮอร์โมนแอนโดรเจนสูงเกินไป การเปลี่ยนแปลงของซีสต์ในรังไข่ และภาวะมีบุตรยาก โรคถุงน้ำในรังไข่หลายใบมีลักษณะเฉพาะคือ โรคอ้วนปานกลาง ประจำเดือนมาไม่ปกติหรือประจำเดือนไม่มา และมีอาการของฮอร์โมนแอนโดรเจนมากเกินไป (ขนดก สิว) รังไข่มักมีซีสต์จำนวนมาก การวินิจฉัยจะอาศัยการทดสอบการตั้งครรภ์ ระดับฮอร์โมน และการตรวจเพื่อแยกเนื้องอกที่ทำให้เกิดอาการ การรักษาจะทำตามอาการ
สาเหตุ โรคถุงน้ำในรังไข่หลายใบ
โรคถุงน้ำในรังไข่หลายใบเป็นโรคทางต่อมไร้ท่อที่พบได้บ่อยในระบบสืบพันธุ์ โดยเกิดขึ้นในผู้ป่วย 5-10% มีลักษณะเฉพาะคือไม่มีไข่ตกและมีแอนโดรเจนมากเกินไปโดยไม่ทราบสาเหตุ รังไข่อาจมีขนาดปกติหรือขยายใหญ่ขึ้น โดยมีแคปซูลเรียบและหนาขึ้น โดยทั่วไป รังไข่จะมีซีสต์ขนาดเล็กจำนวนมากที่มีขนาด 26 มม. บางครั้งอาจพบซีสต์ขนาดใหญ่ที่มีเซลล์เยื่อบุโพรงมดลูกหนาขึ้น ระดับเอสโตรเจนเพิ่มขึ้น ส่งผลให้มีความเสี่ยงต่อภาวะเยื่อบุโพรงมดลูกหนาตัวมากขึ้นและสุดท้ายอาจเป็นมะเร็งเยื่อบุโพรงมดลูก ระดับแอนโดรเจนมักเพิ่มขึ้น ส่งผลให้มีความเสี่ยงต่อภาวะเมตาบอลิกซินโดรมและภาวะขนดกขึ้น
 [ 13 ]
[ 13 ]
กลไกการเกิดโรค
ผู้หญิงที่เป็นโรคถุงน้ำในรังไข่หลายใบ (PCOS) มีความผิดปกติของการเผาผลาญแอนโดรเจนและเอสโตรเจน และการสังเคราะห์แอนโดรเจนบกพร่อง โรคนี้มักมาพร้อมกับระดับฮอร์โมนแอนโดรเจนในซีรั่มที่สูง เช่น เทสโทสเตอโรน แอนโดรสเตอโรนไดโอน ดีไฮโดรเอพิแอนโดรสเตอโรนซัลเฟต และดีเอชอีเอ-เอส อย่างไรก็ตาม บางครั้งอาจสามารถระบุระดับแอนโดรเจนปกติได้
PCOS ยังเกี่ยวข้องกับภาวะดื้อต่ออินซูลิน ภาวะอินซูลินในเลือดสูง และโรคอ้วน ภาวะอินซูลินในเลือดสูงอาจนำไปสู่การยับยั้งการสังเคราะห์ SHBG ซึ่งอาจเพิ่มคุณสมบัติของแอนโดรเจนได้
นอกจากนี้ การดื้อต่ออินซูลินใน PCOS ยังเกี่ยวข้องกับอะดิโปเนกติน ซึ่งเป็นฮอร์โมนที่หลั่งออกมาจากอะดิโปไซต์ที่ควบคุมการเผาผลาญไขมันและระดับน้ำตาลในเลือด
ระดับแอนโดรเจนที่เพิ่มขึ้นจะมาพร้อมกับการเพิ่มขึ้นของผลการกระตุ้นของฮอร์โมน luteinizing (LH) ที่หลั่งออกมาจากต่อมใต้สมองส่วนหน้า ซึ่งนำไปสู่การเจริญเติบโตของเซลล์ theca ของรังไข่ เซลล์เหล่านี้จะเพิ่มการสังเคราะห์แอนโดรเจน (เทสโทสเตอโรน แอนโดรสเตอไดโอน) เนื่องจากระดับฮอร์โมน follicle-stimulating (FSH) ที่ลดลงเมื่อเทียบกับ LH เซลล์เม็ดของรังไข่จึงไม่สามารถเปลี่ยนแอนโดรเจนให้เป็นเอสโตรเจนได้ ซึ่งนำไปสู่การลดลงของระดับเอสโตรเจนและการไม่ตกไข่ในเวลาต่อมา
หลักฐานบางอย่างชี้ให้เห็นว่าผู้ป่วยมีการบกพร่องทางการทำงานของไซโตโครม P450c17 หรือ 17-ไฮดรอกซิเลส ซึ่งยับยั้งการสังเคราะห์แอนโดรเจน
กลุ่มอาการถุงน้ำในรังไข่หลายใบเป็นกลุ่มอาการทางพันธุกรรมที่มีความหลากหลาย การศึกษาสมาชิกในครอบครัวที่มี PCOS พิสูจน์แล้วว่าถ่ายทอดทางพันธุกรรมแบบถ่ายทอดทางยีนเด่น ล่าสุด ได้มีการยืนยันความเชื่อมโยงทางพันธุกรรมระหว่าง PCOS และโรคอ้วนแล้ว ยีน FTO ชนิดหนึ่ง (rs9939609 ซึ่งทำให้เกิดโรคอ้วนโดยทั่วไป) มีความเกี่ยวข้องอย่างมีนัยสำคัญกับความเสี่ยงต่อการเกิด PCOS ความหลากหลายทางพันธุกรรมของตำแหน่ง 2p16 (2p16.3, 2p21 และ 9q33.3) ที่เกี่ยวข้องกับกลุ่มอาการถุงน้ำในรังไข่หลายใบได้รับการระบุแล้ว เช่นเดียวกับยีนที่เข้ารหัสตัวรับฮอร์โมนลูทีไนซิ่ง (LH) และฮอร์โมนโกนาโดโทรปินในมนุษย์ (hCG)
อาการ โรคถุงน้ำในรังไข่หลายใบ
อาการของโรคถุงน้ำในรังไข่หลายใบจะเริ่มขึ้นในช่วงวัยรุ่นและจะค่อยๆ ลดลงเมื่อเวลาผ่านไป การมีประจำเดือนสม่ำเสมอสักระยะหนึ่งหลังจากมีประจำเดือนครั้งแรกจะไม่ถือว่าเป็นโรคถุงน้ำในรังไข่หลายใบ การตรวจร่างกายมักพบเมือกที่ปากมดลูกมาก (ซึ่งบ่งชี้ว่ามีระดับฮอร์โมนเอสโตรเจนสูง) การวินิจฉัยโรคถุงน้ำในรังไข่หลายใบสามารถทำได้หากผู้หญิงมีอาการทั่วไปอย่างน้อย 2 อาการ (โรคอ้วนระดับปานกลาง ขนดก ประจำเดือนมาไม่ปกติ หรือประจำเดือนไม่มา)
อาการทางคลินิกที่พบบ่อยที่สุด ได้แก่:
- ความผิดปกติของรอบเดือน (ประจำเดือนมาไม่ปกติ, เลือดออกผิดปกติจากมดลูก, หยุดการมีประจำเดือนซ้ำ);
- การไม่ตกไข่
- ภาวะมีบุตรยาก;
- ภาวะขนดก
- ความผิดปกติของการเผาผลาญไขมัน (โรคอ้วนและกลุ่มอาการเมตาบอลิก)
- โรคเบาหวาน;
- โรคหยุดหายใจขณะหลับชนิดอุดกั้น
สิ่งที่รบกวนคุณ?
การวินิจฉัย โรคถุงน้ำในรังไข่หลายใบ
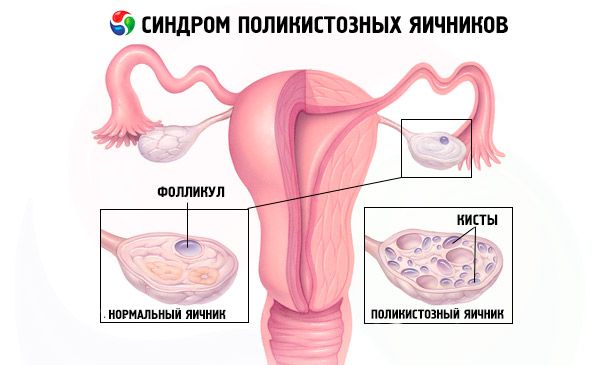
การวินิจฉัยจะทำโดยแยกการตั้งครรภ์ (การทดสอบการตั้งครรภ์) และตรวจระดับเอสตราไดออล FSH TSH และโพรแลกตินในซีรั่มเลือด ยืนยันการวินิจฉัยด้วยอัลตราซาวนด์ ซึ่งพบฟอลลิเคิลมากกว่า 10 ฟอลลิเคิลในรังไข่ ฟอลลิเคิลเหล่านี้มักพบที่บริเวณรอบนอกและมีลักษณะคล้ายสร้อยไข่มุก หากพบฟอลลิเคิลในรังไข่และมีขนดก ควรตรวจระดับฮอร์โมนเทสโทสเตอโรนและดีเอชอีเอเอส ระดับทางพยาธิวิทยาจะประเมินในภาวะหยุดมีประจำเดือน
 [ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ]
[ 23 ], [ 24 ], [ 25 ], [ 26 ], [ 27 ], [ 28 ]
ประวัติและการตรวจร่างกาย
จากการเก็บรวบรวมประวัติอย่างละเอียด จะสามารถระบุปัจจัยทางพันธุกรรมที่ทำให้เกิดโรคถุงน้ำในรังไข่หลายใบได้ ในระหว่างการตรวจร่างกาย จะคำนวณดัชนีมวลกายและอัตราส่วนเอวต่อสะโพก (ปกติ ≤ 0.8) เพื่อวินิจฉัยภาวะน้ำหนักเกินและภาวะอ้วน
โรคถุงน้ำในรังไข่หลายใบมีลักษณะเฉพาะคือมีอาการทางคลินิกและทางห้องปฏิบัติการที่หลากหลาย
วิธีการวินิจฉัยพิเศษสำหรับโรคถุงน้ำรังไข่หลายใบ
การตรวจระดับฮอร์โมนเป็นสิ่งจำเป็นในวันที่ 3-5 ของปฏิกิริยาคล้ายการมีประจำเดือน โดยจะวัดระดับ LH, FSH, โพรแลกติน, เทสโทสเตอโรน, แอนโดรเจนของต่อมหมวกไต - DHEAS, 17-ไฮดรอกซีโปรเจสเตอโรนในเลือด กลุ่มอาการถุงน้ำในรังไข่หลายใบมีลักษณะเฉพาะคือดัชนี LH/FSH สูง -> 2.5-3 (เนื่องจากระดับ LH ที่เพิ่มขึ้น) และภาวะแอนโดรเจนในเลือดสูงเกินไป
เพื่อชี้แจงที่มาของภาวะฮอร์โมนเพศชายสูงเกิน จะทำการทดสอบ ACTH เพื่อวินิจฉัยแยกโรคภาวะฮอร์โมนเพศชายสูงเกินที่เกิดจากการกลายพันธุ์ของยีนที่เข้ารหัสเอนไซม์ 21-hydroxylase ในต่อมหมวกไต (การวินิจฉัยกลุ่มอาการต่อมหมวกไตและอวัยวะสืบพันธุ์แบบแฝงและแบบแฝง) เทคนิค: เวลา 9.00 น. เจาะเลือดจากหลอดเลือดดำบริเวณข้อศอก จากนั้นฉีดซิแนคเธน-ดีโป 1 มก. เข้ากล้ามเนื้อ และหลังจาก 9 ชั่วโมง เจาะเลือดอีกครั้ง ความเข้มข้นของคอร์ติซอลและ 17-hydroxyprogesterone จะถูกกำหนดในเลือดทั้งสองส่วน จากนั้นจะคำนวณค่าสัมประสิทธิ์โดยใช้สูตรพิเศษ ซึ่งค่าไม่ควรเกิน 0.069 ในกรณีเหล่านี้ การทดสอบจะเป็นลบ และผู้หญิง (หรือผู้ชาย) ไม่ใช่พาหะของยีนกลายพันธุ์ 21-hydroxylase
การทดสอบไดเฟนินทำขึ้นเพื่อตรวจหารูปแบบกลางของโรคถุงน้ำในรังไข่หลายใบและความเป็นไปได้ของการรักษาด้วยยาสารสื่อประสาท เทคนิคการทดสอบ: ความเข้มข้นเริ่มต้นของ LH และเทสโทสเตอโรนจะถูกกำหนดในเลือด จากนั้นรับประทานไดเฟนิน 1 เม็ด 3 ครั้งต่อวันเป็นเวลา 3 วัน หลังจากนั้นความเข้มข้นของฮอร์โมนเดียวกันจะถูกกำหนดในเลือดอีกครั้ง การทดสอบจะถือว่าเป็นผลบวกหากระดับของ LH และเทสโทสเตอโรนลดลง
- การอัลตราซาวนด์ของอวัยวะเพศจะพบว่ารังไข่มีขนาดใหญ่ขึ้น (10 ซม.3 หรือมากกว่า) มีฟอลลิเคิลจำนวนมากที่มีเส้นผ่านศูนย์กลางสูงสุด 9 มม. เนื้อเยื่อเกี่ยวพันของรังไข่หนาขึ้น และแคปซูลหนาขึ้น
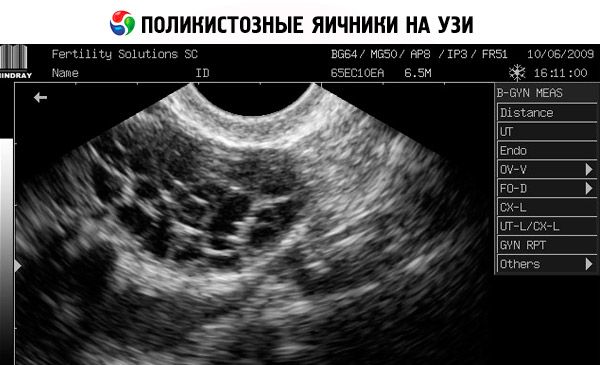
- นอกจากนี้ หากสงสัยว่าเกิดภาวะดื้อต่ออินซูลิน จะมีการทดสอบความทนต่อกลูโคสเพื่อตรวจวัดระดับอินซูลินและกลูโคสก่อนและหลังการออกกำลังกาย
- หากสงสัยว่ามีการเกิดโรคถุงน้ำรังไข่หลายใบจากต่อมหมวกไต ขอแนะนำให้ปรึกษาทางด้านพันธุกรรมและการตรวจจีโนไทป์ HLA
- การตรวจด้วยกล้องตรวจท่อนำไข่และมดลูก
- การส่องกล้อง
- การประเมินความสมบูรณ์ของอสุจิของคู่สมรส
ในเดือนพฤศจิกายน 2558 สมาคมต่อมไร้ท่อคลินิกแห่งอเมริกา (AACE) วิทยาลัยต่อมไร้ท่อแห่งอเมริกา (ACE) และสมาคมต่อมไร้ท่อและ PCOS แห่งฮอร์โมนเพศชาย (AES) ได้ออกแนวทางใหม่สำหรับการวินิจฉัย PCOS แนวทางเหล่านี้มีดังนี้:
- เกณฑ์การวินิจฉัย PCOS จะต้องประกอบด้วยหนึ่งในสามเกณฑ์ต่อไปนี้: ภาวะการตกไข่ไม่ปกติ ภาวะฮอร์โมนแอนโดรเจนสูงทางคลินิก และโรคถุงน้ำในรังไข่หลายใบ
- นอกจากผลการตรวจทางคลินิกแล้ว ควรวัดระดับฮอร์โมน 17-hydroxyprogesterone และแอนตี้มูลเลเรียนในซีรั่มเพื่อวินิจฉัย PCOS
- ระดับฮอร์โมนเทสโทสเตอโรนอิสระมีความไวในการตรวจจับแอนโดรเจนส่วนเกินมากกว่าระดับฮอร์โมนเทสโทสเตอโรนทั้งหมด
สิ่งที่ต้องตรวจสอบ?
ใครจะติดต่อได้บ้าง?
การรักษา โรคถุงน้ำในรังไข่หลายใบ
สตรีที่มีรอบเดือนไม่ตกไข่ (มีประวัติประจำเดือนขาดหรือไม่สม่ำเสมอ และไม่มีหลักฐานของการผลิตโปรเจสเตอโรน) ไม่มีขนดก และไม่มีความปรารถนาที่จะตั้งครรภ์ จะได้รับโปรเจสตินที่เป็นช่วงๆ (เช่น เมดรอกซีโปรเจสเตอโรน 5 ถึง 10 มิลลิกรัม รับประทานครั้งเดียวต่อวัน เป็นเวลา 10 ถึง 14 วันต่อเดือน เป็นเวลา 12 เดือน) หรือยาคุมกำเนิดแบบรับประทานเพื่อลดความเสี่ยงของภาวะเยื่อบุโพรงมดลูกหนาตัวและมะเร็ง และเพื่อลดระดับแอนโดรเจนในกระแสเลือด
สตรีที่มีภาวะถุงน้ำในรังไข่หลายใบที่มีรอบเดือนที่ไม่มีการตกไข่ มีขนดก และไม่ได้วางแผนจะตั้งครรภ์ การรักษาจะมุ่งเป้าไปที่การลดขนดกและควบคุมระดับฮอร์โมนเทสโทสเตอโรนและดีเอชอีเอเอสในซีรั่ม สตรีที่ต้องการตั้งครรภ์จะต้องเข้ารับการรักษาภาวะมีบุตรยาก
การรักษาภาวะมีบุตรยากในกลุ่มอาการถุงน้ำรังไข่หลายใบจะดำเนินการเป็น 2 ระยะ:
- ขั้นที่ 1 - การเตรียมการ;
- ระยะที่ 2 – กระตุ้นการตกไข่
การบำบัดในระยะเตรียมความพร้อมจะขึ้นอยู่กับรูปแบบทางคลินิกและพยาธิวิทยาของโรคถุงน้ำรังไข่หลายใบ
- ในกรณีของโรคถุงน้ำในรังไข่หลายใบและโรคอ้วน แนะนำให้กำหนดยาที่ช่วยลดการดื้อต่ออินซูลิน โดยยาที่เลือกคือเมตฟอร์มิน รับประทานครั้งละ 500 มก. วันละ 3 ครั้ง เป็นเวลา 3–6 เดือน
- ในกรณีของโรคถุงน้ำในรังไข่หลายใบที่มีระดับ LH สูง จะมีการใช้ยาที่ช่วยลดความไวของระบบไฮโปทาลามัส-ต่อมใต้สมองในการยับยั้งการทำงานของรังไข่จนสมบูรณ์ (ระดับเอสตราไดออลในซีรั่ม < 70 พีโมล/ลิตร)
- สเปรย์บูเซอเรลิน 150 มก. ในรูจมูกแต่ละข้าง วันละ 3 ครั้ง ตั้งแต่วันที่ 21 หรือวันที่ 2 ของรอบเดือน รอบ 1–3 เดือน หรือ
- Buserelin Depot ฉีดเข้ากล้ามเนื้อ 3.75 มก. ครั้งเดียวทุก 28 วัน ตั้งแต่วันที่ 21 หรือวันที่ 2 ของรอบเดือน หลักสูตร 1–3 เดือน หรือ
- ลิวโปรเรลินฉีดใต้ผิวหนัง 3.75 มก. ครั้งเดียวทุก 28 วัน ตั้งแต่วันที่ 21 หรือวันที่ 2 ของรอบเดือน ระยะเวลา 1–3 เดือน หรือ
- ทริปโตเรลิน ฉีดใต้ผิวหนัง 3.75 มก. ทุกๆ 28 วัน หรือ 0.1 มก. วันละครั้ง ตั้งแต่วันที่ 21 หรือวันที่ 2 ของรอบประจำเดือน ระยะเวลา 1–3 เดือน
โดยหลักการแล้วไม่สำคัญว่ายา GnRH agonist จะถูกกำหนดให้รับประทานตั้งแต่วันไหน (วันที่ 21 หรือ 2) ของรอบเดือน อย่างไรก็ตาม ควรกำหนดให้รับประทานตั้งแต่วันที่ 21 เนื่องจากในกรณีนี้จะไม่เกิดซีสต์ในรังไข่ หากกำหนดให้รับประทานตั้งแต่วันที่ 2 ของรอบเดือน ระยะการกระตุ้นก่อนระยะการกดการทำงานของยา GnRH นั้นจะตรงกับระยะฟอลลิเคิลของรอบเดือน และอาจทำให้เกิดซีสต์ในรังไข่ได้
ยาทางเลือก:
- เอทินิลเอสตราไดออล/ไดเอโนเจสต์ รับประทาน 30 มก./2 มก. ครั้งเดียวต่อวัน ตั้งแต่วันที่ 5 ถึงวันที่ 25 ของรอบเดือน ระยะเวลา 3–6 เดือน หรือ
- เอทินิลเอสตราไดออล/ไซโปรเทอโรนอะซิเตท รับประทาน 35 มก./2 มก. ครั้งเดียวต่อวัน ตั้งแต่วันที่ 5 ถึงวันที่ 25 ของรอบประจำเดือน ระยะเวลา 3–6 เดือน
- ในกรณีของโรคถุงน้ำรังไข่หลายใบที่มีต่อมหมวกไต การให้ยาที่มีกลูโคคอร์ติคอยด์มีข้อบ่งชี้ดังนี้:
- เดกซาเมทาโซนรับประทาน 0.25–1 มก. ครั้งเดียวต่อวัน เป็นเวลา 3–6 เดือน หรือ
- เมทิลเพรดนิโซโลน รับประทาน 2–8 มก. ครั้งเดียวต่อวัน เป็นเวลา 3–6 เดือน หรือ
- เพรดนิโซโลนรับประทาน 2.5–10 มก. ครั้งเดียวต่อวัน เป็นเวลา 3–6 เดือน
- สำหรับกลุ่มอาการถุงน้ำรังไข่หลายใบแบบส่วนกลาง จะใช้ยากันชัก:
- ไดเฟนิน 1 เม็ด รับประทานวันละ 1-2 ครั้ง;
- คาร์บามาเซพีน รับประทาน 100 มก. วันละ 2 ครั้ง เป็นเวลา 3-6 เดือน
ระยะที่ 2 จะทำการกระตุ้นการตกไข่
การเลือกใช้ยาและแผนการบริหารยาจะพิจารณาจากข้อมูลทางคลินิกและห้องปฏิบัติการ ในระหว่างการกระตุ้นการตกไข่ จะมีการอัลตราซาวนด์และการตรวจติดตามฮอร์โมนของรอบเดือนที่ได้รับการกระตุ้นอย่างระมัดระวัง
การกระตุ้นการตกไข่ด้วยยาใดๆ โดยไม่ได้ติดตามด้วยคลื่นอัลตราซาวนด์ถือเป็นสิ่งที่ยอมรับไม่ได้ ไม่ควรเริ่มการกระตุ้นการตกไข่ในกรณีที่มีซีสต์ในรังไข่ที่มีเส้นผ่านศูนย์กลางมากกว่า 15 มม. และมีความหนาของเยื่อบุโพรงมดลูกมากกว่า 5 มม.
การกระตุ้นการตกไข่ด้วยคลอมีเฟนมีข้อบ่งชี้ในสตรีอายุน้อยที่มีประวัติโรคนี้ในระยะเวลาสั้น และมีระดับเอสโตรเจนที่เพียงพอ (เอสตราไดออลในซีรั่ม < 150 พีโมล/ลิตร) และระดับ LH ต่ำ (> 15 IU/ลิตร)
คลอมีเฟนถูกกำหนดให้รับประทาน 100 มก. ครั้งเดียวต่อวัน ตั้งแต่วันที่ 5 ถึงวันที่ 9 ของรอบประจำเดือน ในเวลาเดียวกันของวัน
การตรวจอัลตราซาวนด์ควบคุมจะทำในวันที่ 10 ของรอบเดือน โดยจะประเมินเส้นผ่านศูนย์กลางของฟอลลิเคิลหลักและความหนาของเยื่อบุโพรงมดลูก การตรวจจะทำทุกวันเว้นวันในช่วงรอบการตกไข่ ขนาดของฟอลลิเคิลหลักไม่ใช่สิ่งสำคัญในวันของรอบเดือน หากเส้นผ่านศูนย์กลางมากกว่า 16 มม. จำเป็นต้องทำอัลตราซาวนด์ทุกวันจนกว่าจะได้ขนาด 20 มม.
รูปแบบการรักษาทางเลือก (ที่มีฤทธิ์ต้านเอสโตรเจนอย่างเด่นชัด):
โครงการที่ 1:
- คลอมีเฟน รับประทาน 100 มก. วันละ 1 ครั้ง ตั้งแต่วันที่ 5 ถึงวันที่ 9 ของรอบเดือน ในเวลาเดียวกันของวัน +
- เอทินิลเอสตราไดออล (EE) รับประทาน 50 มก. วันละ 2 ครั้ง ตั้งแต่วันที่ 10 ถึงวันที่ 15 ของรอบเดือนหรือ
- เอสตราไดออลรับประทาน 2 มก. วันละ 2 ครั้ง ตั้งแต่วันที่ 10 ถึงวันที่ 15 ของรอบประจำเดือน
โครงการที่ 2:
- คลอมีเฟน รับประทาน 100 มก. วันละ 1 ครั้ง ตั้งแต่วันที่ 3 ถึงวันที่ 7 ของรอบเดือน ในเวลาเดียวกันของวัน +
- menotropins ฉีดเข้ากล้ามเนื้อ 75–150 IU ครั้งเดียวต่อวัน ในเวลาเดียวกัน ตั้งแต่วันที่ 7–8 ของรอบเดือน หรือ
- follitropin alpha ฉีดเข้ากล้ามเนื้อ 75–150 IU ครั้งเดียวต่อวัน ในเวลาเดียวกัน เริ่มตั้งแต่วันที่ 7–8 ของรอบประจำเดือน
การกระตุ้นการตกไข่ด้วยคลอมีเฟนซิเตรตไม่ระบุไว้ในสถานการณ์ต่อไปนี้:
- ในภาวะฮอร์โมนเอสโตรเจนต่ำ (ระดับเอสตราไดออลในซีรั่ม < 150 พีโมล/ลิตร)
- หลังจากการเตรียมการเบื้องต้นด้วยตัวกระตุ้น GnRH (เนื่องจากความไวของระบบไฮโปทาลามัส-ต่อมใต้สมอง-รังไข่ลดลง จึงเกิดภาวะเอสโตรเจนต่ำ)
- ในสตรีวัยเจริญพันธุ์ขั้นสูงที่มีประวัติโรคมานานและระดับ LH ในซีรั่มสูง (> 15 IU/L) ไม่เหมาะสมที่จะเพิ่มขนาดคลอมีเฟนเป็น 150 มก./วันในระหว่างการกระตุ้นซ้ำๆ เนื่องจากฤทธิ์ต้านเอสโตรเจนในหลอดเลือดส่วนปลายเชิงลบจะเพิ่มขึ้น
ไม่แนะนำให้กระตุ้นด้วยคลอมีเฟนติดต่อกันเกิน 3 รอบ หากการรักษาไม่ได้ผล ควรใช้โกนาโดโทรปินแทน
การกระตุ้นการตกไข่ด้วยโกนาโดโทรปินนั้นมีข้อบ่งชี้ในกรณีที่ไม่มีการสร้างฟอลลิคูโลซิสเพียงพอหลังจากการกระตุ้นด้วยคลอมีเฟน ในกรณีที่มีฤทธิ์ต้านเอสโตรเจนบริเวณรอบนอกอย่างชัดเจน หรือระดับเอสโตรเจนอิ่มตัวไม่เพียงพอ สามารถทำได้ทั้งในผู้ป่วยอายุน้อยและในวัยเจริญพันธุ์ตอนปลาย
ยาที่เลือก:
- menotropins ฉีดเข้ากล้ามเนื้อ 150–225 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 3–5 ของรอบเดือน ในเวลาเดียวกัน หลักสูตร 7–15 วัน หรือ
- urofollitropin ฉีดเข้ากล้ามเนื้อ 150–225 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 3–5 ของรอบประจำเดือน ในเวลาเดียวกัน ระยะเวลา 7–15 วัน
ยาทางเลือก (สำหรับความเสี่ยงสูงในการเกิดภาวะรังไข่ถูกกระตุ้นเกิน):
- โฟลลิโทรปิน อัลฟา ฉีดเข้ากล้ามเนื้อ 100–150 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 3–5 ของรอบเดือน ในเวลาเดียวกัน ตลอดระยะเวลา 7–15 วัน การกระตุ้นการตกไข่ด้วยโกนาโดโทรปินโดยใช้อนาล็อก GnRH มีข้อบ่งชี้ในกรณีที่มีกลุ่มอาการของรังไข่หลายใบที่มีระดับ LH ในเลือดสูง (> 15 IU/L)
ยาที่เลือก:
- บูเซอเรลินในรูปแบบสเปรย์ 150 มก. ในรูจมูกแต่ละข้าง วันละ 3 ครั้ง ตั้งแต่วันที่ 21 ของรอบเดือน หรือ
- บูเซอเรลิน ดีโป ฉีดเข้ากล้ามเนื้อ 3.75 มก. ครั้งเดียวในวันที่ 21 ของรอบประจำเดือน
- ลิวโปรเรลิน ฉีดใต้ผิวหนัง 3.75 มก. ครั้งเดียวในวันที่ 21 ของรอบประจำเดือน
- ทริปโตเรลิน ฉีดใต้ผิวหนัง 3.75 มก. ครั้งเดียวในวันที่ 21 ของรอบเดือน หรือ 0.1 มก. ครั้งเดียวต่อวันตั้งแต่วันที่ 21 ของรอบเดือน +
- menotropins ฉีดเข้ากล้ามเนื้อ 225–300 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 2–3 ของรอบเดือนถัดไป ในเวลาเดียวกัน
ยาทางเลือก (สำหรับความเสี่ยงสูงในการเกิดภาวะรังไข่ถูกกระตุ้นเกิน):
- menotropins ฉีดเข้ากล้ามเนื้อ 150–225 IU ครั้งเดียวต่อวันตั้งแต่วันที่ 2–3 ของรอบเดือนในเวลาเดียวกันหรือ
- follitropin alpha ฉีดเข้ากล้ามเนื้อ 150–225 IU ครั้งเดียวต่อวันตั้งแต่วันที่ 2–3 ของรอบเดือนในเวลาเดียวกัน +
- ganirelix ฉีดใต้ผิวหนัง 0.25 มก. ครั้งเดียวต่อวัน เริ่มตั้งแต่วันที่ 5–7 ของการใช้โกนาโดโทรปิน (เมื่อรูขุมขนที่เด่นมีขนาด 13–14 มม.)
- cetrorelix ฉีดใต้ผิวหนัง 0.25 มก. ครั้งเดียวต่อวัน เริ่มตั้งแต่วันที่ 5–7 ของการใช้โกนาโดโทรปิน (เมื่อรูขุมขนที่เด่นมีขนาด 13–14 มม.)
การกระตุ้นการตกไข่ในผู้ป่วยในวัยเจริญพันธุ์ตอนปลาย (มีการตอบสนองของรังไข่ต่อยากระตุ้นฮอร์โมนเพศอย่างอ่อน)
ยาที่เลือก:
- menotropins ฉีดเข้ากล้ามเนื้อ 225 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 3 ถึงวันที่ 5 ของรอบเดือน ในเวลาเดียวกัน +
- ทริปโตเรลิน ฉีดใต้ผิวหนัง 0.1 มก. ครั้งเดียวต่อวัน ตั้งแต่วันที่ 2 ของรอบประจำเดือน
ยาทางเลือก:
- ทริปโตเรลิน ฉีดใต้ผิวหนัง 0.1 มก. ครั้งเดียวต่อวัน ตั้งแต่วันที่ 2 ของรอบเดือน +
- follitropin alpha ฉีดเข้ากล้ามเนื้อ 200–225 IU ครั้งเดียวต่อวัน ตั้งแต่วันที่ 3 ถึงวันที่ 5 ของรอบประจำเดือน ในเวลาเดียวกัน
ในทุกแผนการที่ใช้โกนาโดโทรปิน ความเพียงพอของขนาดยาของโกนาโดโทรปินจะถูกประเมินโดยพลวัตของการเจริญเติบโตของรูขุมขน (ปกติคือ 2 มม./วัน) หากรูขุมขนเติบโตช้า ให้เพิ่มขนาดยา 75 IU หากรูขุมขนเติบโตเร็วเกินไป ให้ลดขนาดยาลง 75 IU
ในทุกโครงการ หากมีรูขุมขนที่โตเต็มที่ซึ่งมีขนาด 18–20 มม. และความหนาของเยื่อบุโพรงมดลูกอย่างน้อย 8 มม. จะต้องหยุดการบำบัดและให้ฮอร์โมนโกนาโดโทรปินจากเชื้อเอชไอวีชนิดฮอร์โมนรวมเข้ากล้ามเนื้อในขนาดเดียว 10,000 IU
หลังจากได้รับการยืนยันการตกไข่แล้ว ระยะลูเตียลของรอบเดือนก็จะได้รับการสนับสนุน
ยาที่เลือก:
- ไดโดรเจสเตอโรน รับประทาน 10 มก. วันละ 1-3 ครั้ง เป็นเวลา 10-12 วัน หรือ
- โปรเจสเตอโรนรับประทาน 100 มก. วันละ 2-3 ครั้ง หรือ ฉีดเข้าช่องคลอด 100 มก. วันละ 2-3 ครั้ง หรือ ฉีดเข้ากล้ามเนื้อ 250 มก. วันละ 1 ครั้ง เป็นเวลา 10-12 วัน ยาทางเลือก (ในกรณีที่ไม่มีอาการของการกระตุ้นรังไข่เกิน):
- ฮอร์โมนโกนาโดโทรปินของมนุษย์ชนิดโครริโอนิกฉีดเข้ากล้ามเนื้อ 1,500–2,500 IU ครั้งเดียวต่อวันในวันที่ 3.5 และ 7 ของระยะลูเทียล
ยาอื่นที่ใช้ในการรักษา PCOS:
- สารต้านแอนโดรเจน (เช่น สไปโรโนแลกโทน, ลิวโพรไลด์, ฟินาสเตอไรด์)
- ยาลดน้ำตาลในเลือด เช่น เมตฟอร์มิน อินซูลิน
- ตัวปรับเปลี่ยนตัวรับเอสโตรเจนแบบเลือกสรร (เช่น คลอมีเฟนซิเตรต)
- ยาสิว (เช่น เบนโซอิลเปอร์ออกไซด์, ครีมเทรติโนอิน (0.02-0.1%)/เจล (0.01-0.1%)/สารละลาย (0.05%), ครีมอะดาพาลีน (0.1%)/เจล (0.1%, 0.3%)/สารละลาย (0.1%), อีริโทรไมซิน 2%, คลินดาไมซิน 1%, โซเดียมซัลเฟตาไมด์ 10%)
ผลข้างเคียงของการรักษา
เมื่อใช้คลอมีเฟน ผู้ป่วยส่วนใหญ่จะเกิดผลต่อต้านเอสโตรเจนที่ปลายประสาท ซึ่งประกอบด้วยการเจริญเติบโตของเยื่อบุโพรงมดลูกที่ล่าช้ากว่าการเจริญเติบโตของรูขุมขน และปริมาณเมือกปากมดลูกที่ลดลง เมื่อใช้โกนาโดโทรปิน โดยเฉพาะโกนาโดโทรปินในวัยหมดประจำเดือนของมนุษย์ (เมโนโทรปิน) อาจเกิดกลุ่มอาการรังไข่ถูกกระตุ้นมากเกินไป (OHSS) ได้ เมื่อใช้ FSH แบบรีคอมบิแนนท์ (ฟอลลิโทรปิน อัลฟา) ความเสี่ยงต่อกลุ่มอาการรังไข่ถูกกระตุ้นมากเกินไปจะลดลง เมื่อใช้ยาที่ประกอบด้วยตัวกระตุ้น GnRH (ทริปโตเรลิน บูเซอเรลิน ลิวโปรเรลิน) ความเสี่ยงต่อกลุ่มอาการรังไข่ถูกกระตุ้นมากเกินไปจะเพิ่มขึ้น และการใช้ตัวกระตุ้น GnRH อาจทำให้เกิดอาการขาดเอสโตรเจน เช่น อาการร้อนวูบวาบ ผิวแห้ง และเยื่อเมือก
พยากรณ์
ประสิทธิผลของการรักษาภาวะมีบุตรยากในกลุ่มอาการถุงน้ำรังไข่หลายใบขึ้นอยู่กับลักษณะทางคลินิกและระดับฮอร์โมนของการดำเนินโรค อายุของผู้หญิง ความเหมาะสมของการบำบัดเตรียมความพร้อม และการเลือกแผนการเหนี่ยวนำการตกไข่ที่ถูกต้อง
ในผู้หญิงอายุน้อยร้อยละ 30 ที่มีประวัติโรคนี้เพียงระยะสั้น สามารถตั้งครรภ์ได้หลังการรักษาเตรียมความพร้อมโดยไม่ต้องกระตุ้นการตกไข่
ประสิทธิผลของการกระตุ้นการตกไข่ด้วยคลอมีเฟนไม่เกินร้อยละ 30 ต่อสตรี โดยผู้ป่วยที่เป็นโรคถุงน้ำรังไข่หลายใบร้อยละ 40 จะดื้อต่อคลอมีเฟน
การใช้ยา menotropins และ urofollitropin ช่วยให้ผู้หญิงตั้งครรภ์ได้ 45–50% แต่ยาเหล่านี้จะเพิ่มความเสี่ยงในการเกิดกลุ่มอาการรังไข่ถูกกระตุ้นเกิน
แผนการที่ใช้ GnRH agonists เป็นแผนการที่มีประสิทธิผลมากที่สุด ซึ่งสามารถหลีกเลี่ยง "ปรสิต" LH สูงสุดได้: มากถึง 60% ของการตั้งครรภ์ต่อผู้หญิง อย่างไรก็ตาม เมื่อใช้ยาเหล่านี้ ความเสี่ยงของภาวะแทรกซ้อนสูงสุดจะถูกสังเกตได้ - กลุ่มอาการรังไข่ถูกกระตุ้นมากเกินไปในรูปแบบรุนแรง หรือการตั้งครรภ์แฝด การใช้ยาต้าน GnRH ก็มีประสิทธิผลไม่แพ้กัน แต่ไม่เกี่ยวข้องกับความเสี่ยงสูงของกลุ่มอาการถูกกระตุ้นมากเกินไปของรังไข่
 [ 34 ]
[ 34 ]

