ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
อะไมโลโดซิสของตับ
ตรวจสอบล่าสุด: 29.06.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
อะไมลอยโดซิสเป็นพยาธิสภาพทั่วร่างกายที่มีลักษณะเฉพาะคือมีอะไมลอยด์ (ไกลโคโปรตีนชนิดหนึ่ง) สะสมอยู่ในเนื้อเยื่อและส่งผลให้อวัยวะต่างๆ ในร่างกายทำงานผิดปกติ อะไมลอยโดซิสในตับพบได้น้อยกว่าไตและม้าม [ 1 ] แต่ส่วนใหญ่แล้วมักเกิดร่วมกับความเสียหายต่อร่างกายทั่วร่างกาย เทคนิคการสร้างภาพที่มีอยู่ในปัจจุบันไม่สามารถแสดงการมีอยู่ของอะไมลอยด์ได้อย่างชัดเจน แม้จะสงสัยทางคลินิกและทางรังสีวิทยา การวินิจฉัยอะไมลอยโดซิสก็ยังขึ้นอยู่กับการตัดชิ้นเนื้อเพื่อยืนยันการมีอยู่ของอะไมลอยด์ [ 3 ] การรักษามีความซับซ้อน ครอบคลุม และรวมถึงการใช้ภูมิคุ้มกันและการรักษาตามอาการ ในกรณีที่รุนแรง อาจจำเป็นต้องปลูกถ่ายตับ
ระบาดวิทยา
ความสำเร็จของการรักษาขึ้นอยู่กับการวินิจฉัยโรคอย่างทันท่วงที ซึ่งทำให้เกิดการก่อตัวของโปรตีน-โพลีแซ็กคาไรด์คอมเพล็กซ์ (อะไมลอยด์) ในอวัยวะต่างๆ และตับ จากการปฏิบัติพบว่าอะไมลอยโดซิสนั้นยากที่จะสันนิษฐานหรือสงสัยได้ แม้ว่าจะเป็นไปได้ที่จะระบุและยืนยันได้ก็ตาม ความจริงก็คือ ในกว่า 80% ของกรณีที่ไม่รู้จัก โรคนี้ถูกบดบังทางคลินิกด้วยพยาธิวิทยาของตับ วิธีการวินิจฉัยที่มีประสิทธิภาพที่สุดคือการตรวจชิ้นเนื้อ
อะไมโลโดซิสของตับเป็นปัญหาที่พบได้น้อยกว่าเมื่อเทียบกับอะไมโลโดซิสของไต ในขณะเดียวกัน โรคตับทุกกรณีมักมาพร้อมกับโรคของอวัยวะอื่นด้วย โดยส่วนใหญ่แล้วพยาธิวิทยาจะส่งผลต่อส่วนโครงสร้างของตับสามส่วนเป็นหลัก ซึ่งกำหนดอาการขั้นต่ำและไม่จำเพาะเจาะจง ภาพทางคลินิกและสัณฐานวิทยาของภาวะพร่องเซลล์ตับและความดันเลือดพอร์ทัลสูงนั้นแสดงออกมาในลักษณะพยาธิวิทยาแบบกระจายและแบบ intralobular
การตรวจชิ้นเนื้อตับจะสมเหตุสมผลก็ต่อเมื่อมีตับโตโดยไม่มีอาการตับมาก่อน และไม่มีกลุ่มอาการไต
พบการแพร่กระจายของตับในประมาณร้อยละ 25 ของกรณี และในผู้ป่วยร้อยละ 75 มีเพียงบริเวณพอร์ทัลเทรนเท่านั้นที่ได้รับผลกระทบ
อะไมโลโดซิสขั้นต้นส่งผลต่อตับใน 90% ของกรณี ในขณะที่อะไมโลโดซิสขั้นที่สองส่งผลต่อตับเพียง 47% ของกรณีเท่านั้น
การติดเชื้อที่ตับแบบแยกส่วนนั้นพบได้น้อยมาก ไต (ประมาณ 93% ของกรณี) ม้าม (72%) หัวใจ (57%) ตับอ่อน (36%) ต่อมหมวกไต (29%) ลำไส้ และปอด (21% แต่ละส่วน) มักได้รับผลกระทบพร้อมกัน
ผู้หญิงเป็นโรคนี้บ่อยกว่าผู้ชายเกือบสองเท่า อายุขัยเฉลี่ยของผู้ป่วยอะไมโลโดซิสอยู่ที่ 52-64 ปี
สาเหตุ ของอะไมโลโดซิสในตับ
โรคอะไมลอยโดซิสเกิดขึ้นจากการก่อตัวและการสะสมของคอมเพล็กซ์โพลีแซ็กคาไรด์-โปรตีนที่ซับซ้อน - อะไมลอยด์ - ในเนื้อเยื่อตับ ปัญหาของการเกิดรอยโรคหลักจนถึงปัจจุบันยังไม่ได้รับการศึกษาอย่างเพียงพอ สำหรับพยาธิวิทยารอง มักพบลักษณะที่ปรากฏในโรคดังต่อไปนี้:
- กระบวนการติดเชื้อเรื้อรัง (วัณโรค ซิฟิลิส แอคติโนไมโคซิส)
- กระบวนการอักเสบเป็นหนอง (เยื่อบุหัวใจอักเสบจากจุลินทรีย์, กระดูกอักเสบ, โรคหลอดลมโป่งพอง ฯลฯ);
- โรคมะเร็ง (มะเร็งเม็ดเลือดขาว, มะเร็งอวัยวะภายใน, มะเร็งต่อมน้ำเหลืองชนิดแกรนูโลมาโตซิส)
รูปแบบการตอบสนองของโรคอะไมโลโดซิสพบได้ในผู้ป่วยที่มีหลอดเลือดแข็งร่วมด้วย โรคไขข้ออักเสบ (โรคเบคเทอริว โรคไขข้ออักเสบรูมาตอยด์) โรคสะเก็ดเงิน โรคอักเสบเรื้อรัง และกระบวนการหลายระบบ (รวมถึงโรคซาร์คอยโดซิส) ปัจจัยเสี่ยงหลัก ได้แก่ ความเสี่ยงทางพันธุกรรม ความผิดปกติของภูมิคุ้มกันเซลล์ ภาวะโกลบูลินในเลือดสูง
กลไกการเกิดโรค
มีสมมติฐานหลายประการเกี่ยวกับที่มาของอะไมลอยโดซิสในตับ ผู้เชี่ยวชาญส่วนใหญ่ยึดตามรูปแบบของโปรตีนผิดปกติ ลักษณะทางภูมิคุ้มกันและการกลายพันธุ์ของโรค ตลอดจนการกำเนิดของเซลล์ในบริเวณนั้น การกำเนิดของเซลล์รวมถึงการเปลี่ยนแปลงในปฏิกิริยาที่เกิดขึ้นในระดับเซลล์ (การก่อตัวของเส้นใยตั้งต้นของอะไมลอยด์โดยกลุ่มของแมคโครฟาจ) ถึงแม้ว่าอะไมลอยด์จะก่อตัวและสะสมอยู่ภายนอกโครงสร้างของเซลล์ก็ตาม
ภาวะโปรตีนผิดปกติเกิดจากความจริงที่ว่าอะไมลอยด์เป็นผลจากการเผาผลาญโปรตีนที่ไม่เหมาะสม ปัญหาดังกล่าวมีสาเหตุมาจากภาวะโปรตีนผิดปกติในเลือดและไฟบรินในเลือดสูง ซึ่งนำไปสู่การสะสมของโปรตีนและพาราโปรตีนที่กระจัดกระจายในพลาสมา
ตามทฤษฎีภูมิคุ้มกัน การสร้างอะไมลอยด์เกิดจากปฏิกิริยาแอนติเจน-แอนติบอดี ซึ่งผลิตภัณฑ์จากการสลายตัวของเนื้อเยื่อหรือโปรตีนแปลกปลอมทำหน้าที่เป็นแอนติเจน การสะสมอะไมลอยด์พบได้ส่วนใหญ่ในบริเวณที่มีการสร้างแอนติบอดีและมีแอนติเจนมากเกินไป
นักวิทยาศาสตร์พิจารณาถึงทฤษฎีการกลายพันธุ์ซึ่งคำนึงถึงปัจจัยกลายพันธุ์ต่างๆ ที่สามารถนำไปสู่ความผิดปกติในการสังเคราะห์โปรตีน ซึ่งเป็นทฤษฎีที่มีความเป็นไปได้มากที่สุด
อะไมลอยด์เป็นไฮโปโปรตีนเชิงซ้อนที่ประกอบด้วยโปรตีนทรงกลมและเส้นใยที่รวมกับโพลีแซ็กคาไรด์ การสะสมของอะไมลอยด์ส่งผลต่อชั้นในและชั้นในของเครือข่ายหลอดเลือด เนื้อเยื่อเกี่ยวพันของอวัยวะที่มีเนื้อตับ โครงสร้างของต่อม เป็นต้น การสะสมของอะไมลอยด์ไม่ก่อให้เกิดความเสียหายต่อการทำงาน การสะสมเล็กน้อยไม่ก่อให้เกิดความผิดปกติของการทำงาน แต่เมื่อมีอะไมลอยด์ในตับมาก ปริมาตรจะเพิ่มขึ้น รูปลักษณ์ของอวัยวะเปลี่ยนไป และเกิดการขาดการทำงาน
อะไมลอยโดซิสของตับมีลักษณะเฉพาะคือมีการสะสมของเส้นใยอะไมลอยด์ในช่องว่างของ Dysse ซึ่งโดยปกติจะเริ่มในบริเวณรอบพอร์ทัล แม้ว่าบางครั้งจะอยู่ที่บริเวณศูนย์กลางของหลอดเลือดและอาจสะสมในหลอดเลือดของตับด้วย [ 4 ], [ 5 ] ในกรณีที่รุนแรง การสะสมของอะไมลอยด์จะนำไปสู่การฝ่อของแรงดันในเซลล์ตับ ซึ่งขัดขวางการผ่านของน้ำดี ส่งผลให้เกิดภาวะท่อน้ำดีอุดตัน หรืออาจปิดกั้นไซนัสซอยด์ ส่งผลให้เกิดความดันเลือดสูงในพอร์ทัล [ 6 ], [ 7 ], [ 8 ]
อาการ ของอะไมโลโดซิสในตับ
ภาพทางคลินิกในโรคอะไมลอยโดซิสของตับมีความหลากหลาย ขึ้นอยู่กับความรุนแรงของการสะสมของอะไมลอยด์ คุณสมบัติทางชีวเคมี ระยะเวลาของกระบวนการทางพยาธิวิทยา ระดับของความเสียหายของอวัยวะ และการละเมิดสถานะการทำงานของอวัยวะ
ในระยะแฝงของโรคอะไมลอยโดซิส เมื่อตรวจพบการสะสมของอะไมลอยด์ในตับได้ด้วยการตรวจด้วยกล้องจุลทรรศน์เท่านั้น อาการเริ่มแรกของโรคจะหายเป็นปกติ เมื่อโรคดำเนินไปมากขึ้นและมีการทำงานของอวัยวะบกพร่องมากขึ้น อาการต่างๆ ก็จะค่อยๆ แย่ลง
ตับจะหนาขึ้นและขยายตัวขึ้นเรื่อยๆ วิธีการคลำสามารถเปลี่ยนแปลงได้ แต่ขอบของอวัยวะจะเรียบและไม่เจ็บปวด ในบางครั้งพยาธิวิทยาจะมาพร้อมกับอาการปวดบริเวณใต้ชายโครงด้านขวา อาการอาหารไม่ย่อย ม้ามโต ผิวหนังเหลือง เยื่อเมือกและลูกตาขาว และกลุ่มอาการเลือดออก
อาการที่มีลักษณะเฉพาะมากที่สุดในโรคอะไมโลโดซิสของตับ: [ 9 ], [ 10 ]
- การสะสมอะไมลอยด์ในตับทำให้เกิดตับโตในผู้ป่วยร้อยละ 33-92
- อาการตัวเหลืองเล็กน้อย
- ความดันเลือดพอร์ทัลสูง;
- อาการท่อน้ำดีคั่งปานกลางถึงรุนแรง
เนื่องจากอะไมโลโดซิสแทบจะไม่ส่งผลต่ออวัยวะใดอวัยวะหนึ่งเลย จึงมักมีอาการเพิ่มเติมดังนี้:
- เมื่อไตได้รับความเสียหายจนก่อให้เกิดโรคไตและความดันโลหิตสูง ร่วมกับภาวะไตวายเพิ่มเติม อาการบวมน้ำ บางครั้งอาจเกิดการอุดตันในหลอดเลือดดำของไต เม็ดเลือดขาวในปัสสาวะ เลือดออกในปัสสาวะ โปรตีนในเลือดต่ำ เลือดไปเลี้ยงไตไม่เพียงพอ และอื่นๆ
- เมื่อหัวใจได้รับผลกระทบ จะเกิดอาการที่คล้ายกับกล้ามเนื้อหัวใจหนาตัวผิดปกติ (จังหวะการเต้นผิดปกติ หัวใจโต หัวใจเต้นผิดจังหวะมากขึ้น อ่อนแรงและหายใจลำบาก อาการบวมน้ำ และไม่ค่อยพบมาก เช่น มีของเหลวคั่งในช่องท้องและช่องเยื่อหุ้มปอด เยื่อหุ้มหัวใจอักเสบ)
- หากระบบย่อยอาหารได้รับผลกระทบ อาจเกิดภาวะลิ้นโต อ่อนแรง และหลอดอาหารบีบตัวไม่สะดวก คลื่นไส้และเสียดท้อง ท้องผูกหรือท้องเสีย เป็นต้น
- เมื่อตับอ่อนได้รับผลกระทบ อาการของโรคตับอ่อนอักเสบเรื้อรังจะปรากฏให้เห็น
- หากกลไกของระบบกล้ามเนื้อและโครงกระดูกเข้ามาเกี่ยวข้อง จะเกิดโรคข้ออักเสบหลายเส้นแบบสมมาตร โรคทางข้อมืออักเสบ โรคกล้ามเนื้ออักเสบ และหากระบบประสาทได้รับผลกระทบ จะพบโรคเส้นประสาทอักเสบหลายเส้น อัมพาต ความดันโลหิตต่ำเมื่อลุกยืน เหงื่อออกมากขึ้น และโรคสมองเสื่อม
หากปฏิกิริยาทางพยาธิวิทยาแพร่กระจายไปยังผิวหนัง คราบขี้หูจำนวนมากจะปรากฏขึ้นบนใบหน้า คอ และรอยพับของผิวหนัง ซึ่งอาจรวมถึงโรคผิวหนังอักเสบจากระบบประสาท ไข้ผื่นแดง และโรคผิวหนังแข็ง
การรวมกันของโรคอะไมลอยด์หลายชนิดและอาการต่างๆ ที่หลากหลายทำให้การระบุโรคอะไมลอยโดซิสของตับยากขึ้นมาก และต้องได้รับการวินิจฉัยที่ครอบคลุมและสมบูรณ์
รูปแบบ
จากการจำแนกประเภทของ WHO แบ่งอะไมโลโดซิสออกเป็น 5 ประเภท:
- AL (ประถมศึกษา)
- AA(รอง)
- ATTR (ระบบทางพันธุกรรมและโรคชรา)
- Aβ2M (ในผู้ป่วยที่ต้องฟอกไต)
- AIAPP (ในผู้ป่วยโรคเบาหวานชนิดไม่พึ่งอินซูลิน)
- AB (สำหรับโรคอัลไซเมอร์);
- AANF (โรคอะไมโลโดซิสในผู้สูงอายุ)
มีภาวะอะไมโลโดซิสในตับเฉพาะที่ แต่ส่วนมากจะเป็นโรคที่เกิดขึ้นทั่วร่างกาย ซึ่งกระบวนการทางพยาธิวิทยาจะเกี่ยวข้องกับไต หัวใจ ม้าม ระบบประสาท รวมถึงอวัยวะและเนื้อเยื่ออื่นๆ ด้วย
ภาวะแทรกซ้อนและผลกระทบ
อะไมโลโดซิสในระบบจะค่อยๆ นำไปสู่กระบวนการทางพยาธิวิทยาเฉียบพลันที่อาจนำไปสู่การเสียชีวิตได้ ภาวะแทรกซ้อนที่พบบ่อยที่สุดและเป็นอันตรายถึงชีวิต ได้แก่:
- โรคติดเชื้อที่พบบ่อย (แบคทีเรีย ไวรัส) รวมทั้งปอดบวม ไตอักเสบ ไตอักเสบ
- โรคตับและไตวายเรื้อรัง;
- ภาวะหัวใจล้มเหลวเรื้อรัง (อาจเกิดก่อนกล้ามเนื้อหัวใจตาย)
- โรคหลอดเลือดในสมองแตก
ภาวะหลอดเลือดดำอุดตันเกิดจากการสะสมของโปรตีนบนผนังหลอดเลือดดำ ช่องว่างของหลอดเลือดที่ได้รับผลกระทบจะแคบลง และอวัยวะต่างๆ จะล้มเหลว เมื่อเวลาผ่านไป หลอดเลือดอาจปิดตัวลงอย่างสมบูรณ์เมื่อโปรตีนในเลือดสูงเป็นเวลานาน ภาวะแทรกซ้อนใดๆ ก็ตามอาจนำไปสู่ผลลัพธ์ที่ไม่พึงประสงค์ เช่น เสียชีวิตได้
การวินิจฉัย ของอะไมโลโดซิสในตับ
หากสงสัยว่าเป็นโรคอะไมโลโดซิสของตับ แพทย์จะต้องทำการวินิจฉัยหลังจากปรึกษากับแพทย์ระบบทางเดินอาหารและนักบำบัดโรค แพทย์โรคข้อ แพทย์โรคหัวใจ แพทย์ผิวหนัง แพทย์ระบบประสาท แพทย์ระบบทางเดินปัสสาวะ สิ่งสำคัญคือต้องประเมินประวัติและอาการทางคลินิกอย่างครอบคลุม เพื่อทำการวินิจฉัยทางห้องปฏิบัติการและเครื่องมืออย่างครอบคลุม
การทดสอบจะต้องรวมถึงการตรวจปัสสาวะและเลือด ในโรคอะไมโลโดซิสของตับ มักพบภาวะเม็ดเลือดขาวสูงในปัสสาวะร่วมกับโปรตีนในปัสสาวะและไซลินดรูเรีย และภาวะโปรตีนในเลือดต่ำ ซึ่งส่งผลให้มีไขมันในเลือดสูง โลหิตจาง โซเดียมในเลือดต่ำ และแคลเซียมในเลือดต่ำ และจำนวนเกล็ดเลือดลดลง ตรวจพบพาราโปรตีนในปัสสาวะและอิเล็กโทรโฟรีซิสในซีรั่ม
การวินิจฉัยเครื่องมือประกอบด้วย:
- อีเคจี, เอคโค่;
- อัลตราซาวด์ช่องท้อง;
- เอกซ์เรย์กระเพาะอาหาร หลอดอาหาร;
- การชลประทาน, เอกซเรย์แบเรียม;
- การส่องกล้อง
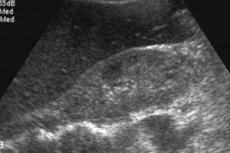
ผลการตรวจทางรังสีวิทยาของอะไมโลโดซิสในตับ ได้แก่ ตับโตแบบไม่จำเพาะ การเพิ่มความถี่ของคลื่นเสียงสะท้อนจากอัลตราซาวนด์หรือความหนาแน่นจากการตรวจเอกซเรย์คอมพิวเตอร์ (CT) และความเข้มของสัญญาณ T1 ที่เพิ่มขึ้นจากการถ่ายภาพด้วยคลื่นแม่เหล็กไฟฟ้า (MRI) [ 12 ] การตรวจด้วย Scintigraphy ร่วมกับตัวบ่งชี้ที่เกี่ยวข้องกับ Tc-99m แสดงให้เห็นการดูดซึมที่ไม่เหมือนกัน แต่ยังไม่จำเพาะ [ 13 ], [ 14 ] GC ได้รับการพิสูจน์แล้วว่าสามารถเพิ่มความแข็งของตับที่วัดโดยอีลาสโตกราฟี [ 15 ], [ 16 ], [ 17 ] แต่มีรายงานกรณีศึกษาเพียงไม่กี่กรณี อีลาสโตกราฟีด้วยคลื่นแม่เหล็กไฟฟ้า (MRE) เป็นวิธีที่ไม่รุกรานที่แม่นยำที่สุดในปัจจุบันในการตรวจหาและระยะของพังผืดในตับ [ 18 ], [ 19 ] MRE มีประโยชน์ในการตรวจจับความก้าวหน้า การตอบสนองต่อการรักษา และการคาดการณ์การเสื่อมของตับในผู้ป่วยที่พังผืดในตับ [ 20 ]
การตรวจอัลตราซาวนด์เพื่อหาภาวะอะไมลอยโดซิสของตับนั้นทำได้ยาก เนื่องจากต้องตรวจพบว่ามีตับโตเกิน 15 ซม. โดยการตรวจชิ้นเนื้อจะดำเนินการภายใต้การควบคุมของอัลตราซาวนด์ ซึ่งถือเป็นตัวบ่งชี้ที่สำคัญในการวินิจฉัยโรค โดยใช้เข็มพิเศษจะเจาะเนื้อเยื่อตับจำนวนเล็กน้อย จากนั้นย้อมด้วยสีย้อมพิเศษและตรวจด้วยกล้องจุลทรรศน์ ซึ่งจะช่วยให้คุณเห็นการสะสมของอะไมลอยด์ได้โดยตรง
การวินิจฉัยที่ชัดเจนจะทำได้หลังจากตรวจพบเส้นใยอะไมลอยด์ในเนื้อเยื่อของตับและอวัยวะอื่นๆ เท่านั้น ชนิดของอะไมลอยโดซิสที่กำหนดโดยพันธุกรรมจะกำหนดโดยการตรวจสอบทางพันธุกรรมและการแพทย์อย่างละเอียดจากสายเลือด
การวินิจฉัยที่แตกต่างกัน
ควรสงสัยอะไมโลโดซิสในผู้ป่วยทุกรายที่มีโปรตีนในปัสสาวะของไต กล้ามเนื้อหัวใจตีบ ระบบประสาทอัตโนมัติหรือปลายประสาทอักเสบ และตับอักเสบ แม้ว่าจะไม่มีพาราโปรตีนโมโนโคลนัลก็ตาม การตรวจสอบประเภทของอะไมโลโดซิสมีความสำคัญมาก เนื่องจากการรักษารอยโรคจากสาเหตุต่างๆ นั้นแตกต่างกันมาก
การวินิจฉัยทางเนื้อเยื่อวิทยาเกี่ยวข้องกับการย้อมด้วย Congo red ตามด้วยการตรวจด้วยกล้องจุลทรรศน์ในแสงโพลาไรซ์ แนะนำให้ทำการตรวจชิ้นเนื้อตัวอย่างเนื้อเยื่อหลายชิ้นในครั้งเดียว หากผลการย้อมเป็นบวก จะทำการวิเคราะห์ภูมิคุ้มกันทางเนื้อเยื่อโดยใช้แอนติบอดีโมโนโคลนอลต่อโปรตีนเบื้องต้นเพื่อระบุประเภทของอะไมลอยด์
การวิเคราะห์ DNA ดำเนินการเพื่อแยกความแตกต่างระหว่างอะไมโลโดซิสขั้นต้นและอะไมโลโดซิสที่ตรวจพบทางพันธุกรรมในรูปแบบต่างๆ สามารถแยกเส้นใยอะไมโลด์จากชิ้นเนื้อที่ถูกตัดออกและเก็บไว้ในกรดอะมิโนแต่ละชนิดได้
การศึกษาเพิ่มเติมเพื่อตรวจสอบภาวะพลาสมาเซลล์ผิดปกติ:
- การวิเคราะห์โปรตีนในซีรั่มของเลือดและปัสสาวะโดยวิธีอิเล็กโทรโฟรีซิส
- อิมมูโนแอสเซย์สำหรับโซ่แสงอิสระ
- การตรึงภูมิคุ้มกัน (immunoblotting) ของโปรตีนในซีรั่ม
- การดูดไขกระดูกและการเจาะเลือดตรวจ
การวินิจฉัยโรคอะไมโลโดซิสของตับเป็นกระบวนการที่ยาวนานและต้องใช้แรงงานมาก ซึ่งต้องอาศัยความใส่ใจที่เพิ่มมากขึ้นจากผู้เชี่ยวชาญและอุปกรณ์ที่มีคุณภาพของคลินิกและห้องปฏิบัติการ
ใครจะติดต่อได้บ้าง?
การรักษา ของอะไมโลโดซิสในตับ
มาตรการการรักษาจะมุ่งเป้าไปที่การลดความเข้มข้นของโปรตีนอะไมลอยด์ที่มีอยู่ก่อนในเลือด (ขจัดสาเหตุของอะไมลอยโดซิส) และสนับสนุนการทำงานของตับให้เพียงพอ
อะไมโลโดซิสทุติยภูมิต้องปิดกั้นกระบวนการอักเสบ (ในโรคติดเชื้อเรื้อรังและโรคภูมิต้านทานตนเอง) ในโรคภูมิต้านทานตนเอง แนะนำให้ใช้ยาต้านเซลล์ เพื่อขจัดกระบวนการติดเชื้อเรื้อรัง มักจะผ่าตัดเอาบริเวณที่อักเสบออก วิธีนี้มักช่วยหยุดการลุกลามของโรคอะไมโลโดซิสและปรับปรุงการทำงานของตับ
ภาวะอะไมโลโดซิสขั้นต้นต้องใช้ยาป้องกันเคมีบำบัดและบางครั้งอาจต้องมีการปลูกถ่ายไขกระดูก
แนวทางปัจจุบันแนะนำให้ใช้ไซโคลฟอสเฟไมด์ บอร์เตโซมิบ เด็กซาเมทาโซน (CyBorD) และดาราทูมูแมบร่วมกันเป็นการรักษาแนวแรกในผู้ป่วยที่เพิ่งได้รับการวินิจฉัยว่าเป็นโรค AL
บอร์เตโซมิบเป็นสารยับยั้งโปรตีเอโซม โปรตีเอโซมมีส่วนเกี่ยวข้องกับการลดพิษต่อโปรตีโอและควบคุมโปรตีนที่ควบคุมความก้าวหน้าของเซลล์และอะพอพโทซิส เซลล์พลาสมาที่สร้างอะไมลอยด์มีความไวต่อการยับยั้งโปรตีเอโซมเป็นพิเศษ เนื่องจากเซลล์เหล่านี้อาศัยโปรตีเอโซมในการลดผลกระทบที่เป็นพิษของห่วงโซ่แสงและป้องกันอะพอพโทซิส
Daratumumumab เป็นแอนติบอดีโมโนโคลนอล (mAb) ที่จับกับ CD38 ซึ่งเป็นไกลโคโปรตีนที่ผ่านเยื่อหุ้มเซลล์ซึ่งแสดงออกบนพื้นผิวของเซลล์พลาสมา ทำให้เกิดอะพอพโทซิส เป็นยาตัวเดียวที่ได้รับการอนุมัติโดยเฉพาะสำหรับการรักษาอะไมโลโดซิส AL เมื่อใช้ร่วมกับ CyBorD ประสิทธิภาพของ CyBorD-daratumumumab นั้นสูงมาก โดยผู้ป่วย 78% มีการตอบสนองทางโลหิตวิทยาอย่างมีนัยสำคัญ (กำหนดเป็นการตอบสนองอย่างสมบูรณ์หรือการตอบสนองบางส่วนที่ดีมาก) อัตราการรอดชีวิตเฉลี่ยในกลุ่มผู้ป่วยขนาดเล็กที่ได้รับ CyBorD (n = 15) คือ 655 วัน เมื่อเทียบกับ 178 วันสำหรับผู้ป่วยที่ได้รับการรักษาด้วยเมลฟาแลน-เดกซาเมทาโซนอื่นๆ (n = 10) 4
อย่างไรก็ตาม การบำบัดเหล่านี้มีผลข้างเคียงมากมาย รวมทั้งความเป็นพิษต่อหัวใจ ซึ่งนำไปสู่ความจำเป็นต้องลดขนาดยาหรือระงับการรักษา และต้องใช้กลยุทธ์การบำบัดอื่นๆ ที่มีประสิทธิภาพน้อยกว่าแต่สามารถทนได้มากกว่า
Isatuximab ซึ่งเป็นแอนติบอดีโมโนโคลนอลต่อ CD38 ที่คล้ายกับ daratumumab กำลังถูกศึกษาเพื่อใช้ในการรักษาโรคพลาสมาเซลล์ดิสเครเซียซึ่งเป็นสาเหตุของ AL
ปัจจุบันมีการศึกษาแอนติบอดีโมโนโคลนัลสามชนิด ได้แก่ บิร์ตามิแมบ CAEL-101 และ AT-03 เพื่อกำจัดใยอะไมลอยด์ออกจากอวัยวะที่เป็นโรค ผลการศึกษาเหล่านี้จะสามารถให้หลักฐานโดยตรงสำหรับสมมติฐานที่ว่าการกำจัดใยอะไมลอยด์ที่สะสมในห่วงโซ่เบาออกจากอวัยวะต่างๆ จะทำให้การทำงานของอวัยวะดีขึ้น [ 21 ]
เพื่อสนับสนุนการทำงานของตับ แพทย์จึงสั่งจ่ายยาที่มีกรดเออร์โซ-ดีออกซีโคลิกเป็นส่วนประกอบ (ตัวอย่าง - เออร์โซซาน) กรดเออร์โซ-ดีออกซีโคลิกช่วยทำให้เยื่อหุ้มเซลล์มีเสถียรภาพ ลดผลเสียของกรดไขมันที่เป็นพิษต่อภาวะคั่งของน้ำดีที่เกิดจากการสะสมของอะไมลอยด์ และช่วยฟื้นฟูการไหลของน้ำดีให้เป็นปกติ
นอกจากนี้ ยังมีการบำบัดตามอาการและการสนับสนุนการทำงานของโครงสร้างที่สำคัญอื่นๆ เช่น ระบบประสาท หัวใจ ไต เป็นต้น การบำบัดแบบสนับสนุนสำหรับผู้ป่วยโรคอะไมโลโดซิสของตับประกอบด้วยการรักษาทางคลินิกต่างๆ เช่น การรักษาภาวะหัวใจล้มเหลว หัวใจเต้นผิดจังหวะ ความผิดปกติของการนำไฟฟ้า ภาวะลิ่มเลือดอุดตัน และการมีอาการตีบของหลอดเลือดแดงใหญ่ร่วมด้วย
การรักษาอื่นๆ ขึ้นอยู่กับประเภทของอะไมโลโดซิสและส่วนต่างๆ ของร่างกายที่ได้รับผลกระทบ การรักษาอาจรวมถึง: [ 22 ]
- ยาบรรเทาอาการ เช่น ยาแก้ปวด ยาแก้คลื่นไส้ หรือยาลดอาการบวม (ยาขับปัสสาวะ)
- ยาเพื่อลดระดับอะไมลอยด์
- การฟอกไต;
- การปลูกถ่ายตับ
ตับผลิต TTR (ทรานสไธเรติน ซึ่งเป็นโปรตีนที่เกี่ยวข้องกับการขนส่งไทรอกซิน (T4) และโปรตีนที่จับกับเรตินอล ทรานสไธเรตินสังเคราะห์ส่วนใหญ่ในตับและอุดมไปด้วยสายเบต้าซึ่งมีแนวโน้มที่จะรวมตัวกันเป็นเส้นใยอะไมลอยด์ที่ไม่ละลายน้ำ) ซึ่งวัดได้ในซีรั่ม ดังนั้น การปลูกถ่ายตับจึงได้รับการแนะนำมาโดยตลอด (ตั้งแต่ปี 1990) ให้เป็นการรักษาขั้นแรกเพื่อกำจัดแหล่งหลักของ TTR อะไมลอยด์ในผู้ป่วยที่มีรูปแบบทางพันธุกรรม (ATTRv) ในขณะที่รูปแบบ ATTR-wt ไม่ได้ระบุไว้ การปลูกถ่ายตับในผู้ป่วยอายุน้อยในระยะเริ่มต้นของโรคเกี่ยวข้องกับอัตราการรอดชีวิตที่สูง 20 ปี การปลูกถ่ายตับดูเหมือนว่าจะมีประสิทธิภาพมากกว่าในการกลายพันธุ์บางอย่างและมีประสิทธิผลน้อยกว่าในบางอย่าง เช่น V122I (ที่เกี่ยวข้องกับกล้ามเนื้อหัวใจ) การปลูกถ่ายตับและหัวใจร่วมกันยังเป็นไปได้สำหรับผู้ป่วย ATTRv อายุน้อยที่มีภาวะกล้ามเนื้อหัวใจผิดปกติ โดยข้อมูลจากวรรณกรรมเกี่ยวกับผู้ป่วยกลุ่มเล็กแสดงให้เห็นว่าการปลูกถ่ายทั้งสองวิธีนี้มีการพยากรณ์โรคที่ดีกว่าการปลูกถ่ายหัวใจเพียงอย่างเดียว
ห้ามใช้ผู้ป่วยที่เป็นโรคอะไมลอยโดซิสในตับโดยเด็ดขาด เนื่องจากไกลโคไซด์ของหัวใจและสารยับยั้งแคลเซียม เช่น ไดลเทียเซมหรือเวอราพามิล ซึ่งอาจสะสมอยู่ในอะไมลอยด์ได้ ควรใช้ยา ACE inhibitor และ beta-adrenoblocker ด้วยความระมัดระวัง
ในกรณีความดันโลหิตตกเมื่อลุกยืน แพทย์จะสั่งจ่ายมิเนอรัลคอร์ติคอยด์หรือกลูโคคอร์ติโคสเตียรอยด์ เนื่องจากยาเหล่านี้อาจทำให้เกิดภาวะหัวใจล้มเหลวได้ นอกจากนี้ ยังต้องใช้มิโดดรีนอัลฟา-อะดรีโนมิเมติก (กูทรอน) ด้วยความระมัดระวัง
ยากันชักและยาแก้ซึมเศร้าเหมาะสำหรับผู้ป่วยโรคเส้นประสาท
ในกรณีของโรคอะไมโลโดซิสของตับบางกรณี แพทย์จะต้องพิจารณาทำการปลูกถ่ายอวัยวะ
การป้องกัน
เนื่องจากขาดข้อมูลเกี่ยวกับพยาธิสภาพของโรคอะไมโลโดซิสในตับ ผู้เชี่ยวชาญจึงไม่สามารถพัฒนาวิธีป้องกันโรคนี้โดยเฉพาะได้ ดังนั้น ความพยายามหลักจึงลดลงเหลือเพียงการตรวจจับและรักษาโรคเรื้อรังที่อาจกระตุ้นให้เกิดโรคนี้อย่างทันท่วงที หากมีกรณีของโรคอะไมโลโดซิสในตำแหน่งใดตำแหน่งหนึ่งในครอบครัว แนะนำให้ไปพบแพทย์เพื่อตรวจร่างกายที่คลินิกอย่างเป็นระบบ
โดยทั่วไป การป้องกันมักจะลดน้อยลงเหลือเพียงการกำจัดโรคติดเชื้ออย่างทันท่วงที โดยเฉพาะโรคที่มีแนวโน้มจะกลายเป็นโรคเรื้อรัง การป้องกันการเกิดวัณโรค การติดเชื้อในปอด เป็นต้น การตรวจจับและการรักษาที่เหมาะสมของการติดเชื้อสเตรปโตค็อกคัสอย่างทันท่วงทีจึงมีความสำคัญ เนื่องจากอาจเป็นสาเหตุของกระบวนการอักเสบเรื้อรังที่เกิดจากภูมิคุ้มกันทำลายตนเองได้ เรากำลังพูดถึงโรคสการ์ลาตินา ต่อมทอนซิลอักเสบจากสเตรปโตค็อกคัส เป็นต้น
หากผู้ป่วยมีโรคภูมิคุ้มกันบกพร่องอยู่แล้ว ควรไปพบแพทย์อย่างสม่ำเสมอ สังเกตการทำงานของพยาธิวิทยา ใช้ยาตามที่แพทย์กำหนด และปรับขนาดยาตามข้อบ่งชี้
พยากรณ์
การพยากรณ์โรคสำหรับผู้ป่วยโรคอะไมโลโดซิสในตับนั้นไม่ดีนัก โรคจะค่อยๆ รุนแรงขึ้นเรื่อยๆ จนในที่สุดจะทำให้ระบบอวัยวะที่ได้รับผลกระทบทำงานผิดปกติและเสียชีวิตได้ โดยเฉพาะอย่างยิ่งหากระบบอวัยวะล้มเหลว
ผู้ป่วยที่มีพยาธิสภาพระบบส่วนใหญ่มักเสียชีวิตจากภาวะไตวายเรื้อรัง แม้ว่าในบางกรณี การฟอกไตหรือการฟอกไตทางช่องท้องแบบต่อเนื่องจะช่วยให้การพยากรณ์โรคของผู้ป่วยดีขึ้นก็ตาม อัตราการรอดชีวิตของผู้ป่วยที่ฟอกไตไม่ว่าจะชนิดใดสามารถเปรียบเทียบได้กับผู้ป่วยที่มีพยาธิสภาพระบบอื่นๆ และโรคเบาหวาน
สาเหตุหลักของการเสียชีวิตระหว่างการฟอกไต คือ การเกิดภาวะแทรกซ้อนจากระบบหัวใจและหลอดเลือด
การปลูกถ่ายตับถือเป็นวิธีการรักษาโรคหลักวิธีหนึ่งมาช้านาน และอัตราการรอดชีวิตที่คาดหวังได้มากที่สุดคือในผู้ป่วยที่มีอายุไม่เกิน 50 ปี (โดยต้องให้กระบวนการทางพยาธิวิทยาเกิดขึ้นในช่วงสั้นๆ และดัชนีมวลกายอยู่ในเกณฑ์ปกติ) ผู้ป่วยที่มีภาวะอะไมโลโดซิสของตับร่วมกับโรคเส้นประสาทส่วนปลายมีแนวโน้มว่าจะมีอาการแย่ลงเล็กน้อย

