ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
บทบาทของการเปลี่ยนแปลงของกระดูกใต้กระดูกอ่อนในการเกิดโรคข้อเข่าเสื่อม
ตรวจสอบล่าสุด: 04.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
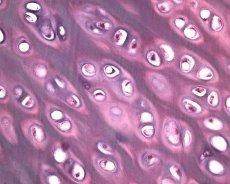
นอกจากการเสื่อมของกระดูกอ่อนแล้ว เนื้อเยื่อกระดูกที่อยู่ข้างใต้ยังมีส่วนเกี่ยวข้องในกระบวนการทางพยาธิวิทยาของโรคข้อเสื่อมอีกด้วย สันนิษฐานว่าการหนาตัวของแผ่นกระดูกใต้กระดูกอ่อนมีส่วนทำให้โรคข้อเสื่อมลุกลาม เมื่อโรคข้อเสื่อมลุกลาม กระดูกอ่อนใต้กระดูกอ่อนซึ่งต้องรับแรงกดทางกลและเคมีจะสึกกร่อนลงอย่างช้าๆ เนื่องจากความไม่สมดุลในกระบวนการสลายและซ่อมแซมกระดูกอ่อน โดยเฉพาะอย่างยิ่ง แรงกดทางกลที่เกี่ยวข้องกับข้อต่อที่ "รับ" น้ำหนักของร่างกายจะส่งผลให้เกิดการแตกร้าวเล็กๆ จำนวนมากในแผ่นกระดูกใต้กระดูกอ่อนและกระดูกอ่อน เมื่อกระดูกอ่อนใต้กระดูกอ่อนสึกกร่อน กระดูกใต้กระดูกอ่อนก็จะแข็งตัวมากขึ้น ความแข็งของเนื้อเยื่อกระดูกจะเพิ่มขึ้น ซึ่งส่งผลให้โครงสร้างของกระดูกอ่อนใต้กระดูกอ่อนถูกทำลายมากขึ้น อย่างไรก็ตาม คำถามเกี่ยวกับลักษณะหลักหรือรองของการเปลี่ยนแปลงของกระดูกใต้กระดูกอ่อนในโรคข้อเสื่อมยังคงไม่มีคำตอบ
จนกระทั่งเมื่อไม่นานมานี้ การเปลี่ยนแปลงที่ตรวจพบทางรังสีในสารฟองน้ำของกระดูกใต้กระดูกอ่อน เช่น สเคลอโรซิส หรือการก่อตัวของซีสต์ ถือเป็นผลรองในผู้ป่วยโรคข้อเสื่อมอย่างไรก็ตาม ผลการศึกษาทางคลินิกและการทดลองบ่งชี้ว่ากระดูกใต้กระดูกอ่อนอาจมีบทบาทในการเกิดโรคข้อเสื่อมได้ กลไกที่เป็นไปได้อย่างหนึ่งคือการเพิ่มขึ้นอย่างรวดเร็วของระดับความแข็งของกระดูกใต้กระดูกอ่อนเนื่องมาจากความสมบูรณ์ของเนื้อเยื่อกระดูกอ่อนที่อยู่ด้านล่างขึ้นอยู่กับคุณสมบัติเชิงกลของ "ฐาน" ของกระดูก การศึกษาในไพรเมตแสดงให้เห็นว่าการเปลี่ยนแปลงในกระดูกใต้กระดูกอ่อนสามารถเกิดขึ้นก่อนการเปลี่ยนแปลงในกระดูกอ่อนข้อต่อ หลักฐานที่สนับสนุนและคัดค้านสมมติฐานนี้ซึ่งปรากฏขึ้นจากการศึกษาในสัตว์ทดลองเกี่ยวกับโรคข้อเสื่อมและการศึกษาทางคลินิกได้ทำให้การถกเถียงกันรุนแรงขึ้นเท่านั้น การหนาตัวของทราเบคูลาในกระดูกใต้กระดูกอ่อนไม่ได้มาพร้อมกับการเพิ่มขึ้นของแร่ธาตุในกระดูกเสมอไป หรืออีกนัยหนึ่งคือการเพิ่มขึ้นของปริมาตรของออสทียด์ สัญญาณของการสร้างแคลเซียมที่ผิดปกตินี้บ่งชี้ว่าการรบกวนการควบคุมการสร้างกระดูกใหม่เป็นส่วนสำคัญของโรคข้อเข่าเสื่อม และยังสนับสนุนแนวคิดเรื่องข้อบกพร่องของเซลล์กระดูกในโรคข้อเข่าเสื่อม กลุ่มของ J. Dequeker (1989) ถือว่าโรคข้อเข่าเสื่อมเป็น "โรคกระดูกที่เกิดจากการเผาผลาญโดยทั่วไป"
เนื้อเยื่อกระดูกจะถูกสร้างขึ้นใหม่ตลอดเวลา กระบวนการไดนามิกนี้เรียกว่าการปรับโครงสร้างกระดูก ซึ่งเป็นลำดับการดูดซับและการสร้างแร่ธาตุที่ซับซ้อน เซลล์สลายกระดูกจะดูดซับเนื้อเยื่อกระดูก และเซลล์สร้างกระดูกจะหลั่งโปรตีนที่สร้างองค์ประกอบอินทรีย์หลักในการสร้างแร่ธาตุ การสร้างและการดูดซึมของกระดูกไม่ได้เกิดขึ้นโดยสุ่มทั่วทั้งโครงกระดูก แต่เป็นกระบวนการที่ได้รับการตั้งโปรแกรมไว้ซึ่งเกิดขึ้นในบริเวณต่างๆ ของโครงกระดูก เรียกว่าหน่วยสร้างกระดูกใหม่ ในช่วงต้นของวงจร เซลล์สลายกระดูกจะปรากฏบนพื้นผิวที่ไม่ได้ใช้งาน ภายใน 2 สัปดาห์ เซลล์เหล่านี้จะสร้างอุโมงค์ในกระดูกคอร์เทกซ์หรือช่องว่างบนพื้นผิวของกระดูกเนื้อกระดูก ความถี่ในการเปิดใช้งานหน่วยสร้างกระดูกใหม่จะกำหนดระดับการสร้างกระดูกใหม่ ในคนหนุ่มสาวที่มีสุขภาพแข็งแรง กระบวนการสร้างและการดูดซึมของกระดูกจะสมดุลกัน และมวลกระดูกจะคงอยู่เป็นปกติ ในการควบคุมการสลายของเนื้อเยื่อกระดูกด้วยฮอร์โมน อย่างน้อย PTH และ PGE2 ไม่เพียงแต่กระดูกอ่อนเท่านั้นแต่ ยังรวมถึงกระดูกอ่อนด้วย เนื่องจากภายใต้อิทธิพลของฮอร์โมนเหล่านี้ ปัจจัยที่กระตุ้นการสลายของกระดูกโดยกระดูกอ่อนจะถูกปล่อยออกมา ปัจจุบัน มีตัวควบคุมการเจริญเติบโตของเนื้อเยื่อกระดูกทั้งในระดับท้องถิ่นและระดับระบบมากกว่า 12 ตัวที่ทราบกันดีว่ามีผลต่อการปรับโครงสร้างใหม่ โดยเฉพาะ PTH, 1,25(OH) 2D3 ,แคลซิโทนิน, ฮอร์โมนการเจริญเติบโต, กลูโคคอร์ติคอยด์, ฮอร์โมนไทรอยด์, อินซูลิน, IGF (1 และ 2), เอสโตรเจน, PGE2 และแอนโดรเจน
เซลล์กระดูกจะปล่อยโปรตีนและไซโตไคน์จำนวนหนึ่งที่ทำหน้าที่ควบคุมต่อมไร้ท่อและถ่ายทอดสัญญาณ โปรตีนที่ผลิตโดยออสติโอบลาสต์ ได้แก่ โปรตีนเมทริกซ์ของกระดูก เช่น คอลลาเจน ออสเตโอพอนติน ออสเตโอแคลซิน ไซอาโลโปรตีนของกระดูก นอกจากนี้ เซลล์เหล่านี้ยังปล่อยโปรตีเอสในรูปแบบทั้งแบบทำงานและแบบแฝงที่มีส่วนร่วมในกระบวนการสร้างเนื้อเยื่อกระดูกใหม่ ซึ่งก็คือ MMP ซึ่งเป็นส่วนประกอบของระบบพลาสมินเจนแอคติเวเตอร์ (PA)/พลาสมิน ไซโตไคน์ที่ออสติโอบลาสต์ปล่อยออกมาสามารถออกฤทธิ์ได้ทั้งผ่านกลไกออโตไครน์และเส้นทางพาราไครน์บนเซลล์ในบริเวณนั้น (ออสติโอบลาสต์อื่น ออสติโอคลาสต์)
ยังไม่ทราบว่าสัญญาณเหล่านี้ถูกควบคุมโดยความเครียดทางกลหรือสัญญาณเคมีอื่นๆ ที่เกิดจากความเครียดทางกลหรือไม่ อย่างไรก็ตาม เป็นที่ทราบกันดีว่าความเครียดทางกลซ้ำๆ ทำให้เซลล์กระดูกและ/หรือโปรตีนขยายตัวในบริเวณนั้น ในร่างกาย การรับแรงทางกลสามารถกระตุ้นเซลล์สร้างกระดูก เพิ่มระดับของนิวคลีโอไทด์แบบวงแหวน การผลิตพรอสตาแกลนดิน และทำให้เกิดการเปลี่ยนแปลงทางสัณฐานวิทยาที่เกี่ยวข้องกับการปรับโครงสร้างของกระดูก ในหลอดทดลอง ความเครียดทางกลทำให้เซลล์สร้างกระดูกขยายตัว การแสดงออกของ mRNA ของโปรตีนกระดูกที่เกี่ยวข้องกับการสร้างและการสร้างกระดูก การปลดปล่อยปัจจัยการเจริญเติบโตในบริเวณนั้น เช่น IGF-1 และ IGF-2 และโมเลกุลการยึดเกาะ การส่งสัญญาณความเครียดทางกลสามารถดำเนินการได้ผ่านช่องไอออนที่ไวต่อแรงกล
มีหลักฐานทางอ้อมของความผิดปกติของออสทีโอบลาสต์ในโรคข้อเสื่อม G. Gevers และ J. Dequeker (1987) แสดงให้เห็นถึงการเพิ่มขึ้นของระดับออสทีโอแคลซินในซีรั่มในผู้หญิงที่มีโรคข้อเสื่อมที่มือ รวมถึงในเนื้อเยื่อปลูกถ่ายกระดูกเปลือกสมอง ซึ่งบ่งชี้ว่าพยาธิสภาพของกระดูกอาจเป็นส่วนหนึ่งของโรคข้อเสื่อม การชันสูตรพลิกศพเผยให้เห็นไม่เพียงแต่กระดูกใต้กระดูกอ่อนหนาขึ้นเท่านั้น แต่ยังพบปริมาณแร่ธาตุที่ต่ำผิดปกติที่หัวกระดูกต้นขาอีกด้วย ในหนูตะเภาที่มีโรคข้อเสื่อมที่เกิดจากการผ่าตัด การตรวจเอกซเรย์คอมพิวเตอร์เผยให้เห็นว่าเศษส่วนของกระดูกในบริเวณใต้กระดูกอ่อนหนาขึ้นอย่างมีนัยสำคัญ ความไม่สมดุลระหว่างคอลลาเจนและโปรตีนที่ไม่ใช่คอลลาเจน (ออสทีโอแคลซิน เป็นต้น) อาจทำให้ปริมาตรของกระดูกเพิ่มขึ้น แต่ไม่ส่งผลต่อความหนาแน่นของแร่ธาตุในกระดูก ตามรายงานของ M. Shimizu et al. (1993) ความก้าวหน้าของการเปลี่ยนแปลงที่เสื่อมในกระดูกอ่อนข้อต่อมีความเกี่ยวข้องกับการปรับเปลี่ยนโครงสร้างกระดูกใต้กระดูกอ่อนอย่างเข้มข้นมากขึ้นและความแข็งแกร่งที่เพิ่มขึ้น ซึ่งยังบ่งบอกถึงข้อบกพร่องในเซลล์เนื้อเยื่อกระดูกในโรคข้อเสื่อมอีกด้วย ตามสมมติฐานที่เสนอโดย B. Lee และ M. Aspden (1997) การแบ่งตัวของเซลล์กระดูกที่บกพร่องสามารถนำไปสู่ความแข็งแกร่งของเนื้อเยื่อกระดูกที่เพิ่มขึ้น แต่ไม่ได้ทำให้ความหนาแน่นของแร่ธาตุเพิ่มขึ้น
CI Westacott et al. (1997) ตั้งสมมติฐานว่าเซลล์สร้างกระดูกที่ผิดปกติส่งผลโดยตรงต่อการเผาผลาญของกระดูกอ่อน จากการเพาะเลี้ยงเซลล์สร้างกระดูกจากผู้ป่วยโรคข้อเสื่อมที่มีเซลล์กระดูกอ่อนจากผู้ที่ไม่มีโรคข้อ ผู้เขียนสังเกตเห็นการเปลี่ยนแปลงที่สำคัญในการปล่อยไกลโคสะมิโนไกลแคนโดยเนื้อเยื่อกระดูกอ่อนปกติในหลอดทดลอง แต่ระดับการปล่อยไซโตไคน์ยังคงไม่เปลี่ยนแปลง G. Hilal et al. (1998) แสดงให้เห็นว่าการเพาะเลี้ยงเซลล์สร้างกระดูกจากกระดูกใต้กระดูกอ่อนของผู้ป่วยโรคข้อเสื่อมในหลอดทดลองมีการเผาผลาญที่เปลี่ยนแปลงไป โดยกิจกรรมของระบบ AP/plasmin และระดับ IGF-1 ในเซลล์เหล่านี้เพิ่มขึ้น การสังเกตของ CI Westacott et al. (1997) สามารถอธิบายได้จากการเพิ่มขึ้นของกิจกรรมของโปรตีเอสในเซลล์กระดูกใต้กระดูกอ่อน
ยังไม่ทราบแน่ชัดว่าการเปลี่ยนแปลงในกระดูกใต้กระดูกอ่อนเป็นจุดเริ่มต้นของโรคข้อเข่าเสื่อมหรือมีส่วนทำให้โรคลุกลาม DK Dedrick และคณะ (1993) แสดงให้เห็นว่าในสุนัขที่มีโรคข้อเข่าเสื่อมที่เกิดจากการผ่าตัด การหนาตัวของกระดูกใต้กระดูกอ่อนไม่ใช่เงื่อนไขที่จำเป็นสำหรับการพัฒนาของการเปลี่ยนแปลงคล้ายโรคข้อเข่าเสื่อมในกระดูกอ่อน แต่มีส่วนทำให้กระบวนการเสื่อมในกระดูกอ่อนดำเนินไป ผลการศึกษาของ A. Sa'ied และคณะ (1997) ขัดแย้งกับข้อมูลของการศึกษาครั้งก่อน โดยใช้เอคโคกราฟีความถี่ 50 เมกะเฮิรตซ์ในการประเมินการเปลี่ยนแปลงทางสัณฐานวิทยาเบื้องต้นและความก้าวหน้าในกระดูกอ่อนข้อและกระดูกในโรคข้อเข่าเสื่อมที่เกิดจากการฉีดกรดโมโนไอโอโดอะซิติกเข้าในข้อเข่าของหนู ผู้เขียนได้สาธิตกระบวนการพร้อมกันของการเปลี่ยนแปลงในกระดูกและกระดูกอ่อนในช่วงสามวันแรกหลังการฉีด
เซลล์กระดูกอ่อนจะหลั่งปัจจัยการเจริญเติบโตและไซโตไคน์ที่เกี่ยวข้องกับการปรับโครงสร้างของกระดูกในบริเวณนั้น ซึ่งอาจส่งเสริมการปรับโครงสร้างของกระดูกอ่อนที่เหมาะสมในข้อ "รับน้ำหนัก" หลังจากที่เซลล์กระดูกอ่อนแทรกผ่านรอยแตกร้าวเล็กๆ ในชั้นกระดูกอ่อนที่มีแคลเซียมเกาะอยู่ นอกจากนี้ ยังพบผลิตภัณฑ์ที่หลั่งจากเซลล์กระดูกในของเหลวในข้อ ผลิตภัณฑ์ที่น่าจะเป็นไปได้มากที่สุดที่เซลล์กระดูกอ่อนผิดปกติจะหลั่งออกมา ซึ่งสามารถเริ่มกระบวนการปรับโครงสร้างของกระดูกอ่อนในบริเวณนั้นได้ คือ TGF-b และโปรตีนมอร์โฟเมตริกของกระดูก (BMP) เซลล์กระดูกอ่อนและเซลล์กระดูกอ่อนจะหลั่งโปรตีนทั้งสองชนิดในตระกูล TGF และทั้งสองชนิดสามารถปรับเปลี่ยนโครงสร้างของกระดูกและกระดูกอ่อนได้ J. Martel Pelletier และคณะ (1997) สังเกตเห็นการเพิ่มขึ้นของระดับ TGF-β ในชิ้นส่วนกระดูกใต้กระดูกอ่อนของผู้ป่วยโรคข้อเสื่อมเมื่อเทียบกับผู้ที่มีสุขภาพแข็งแรง ซึ่งบ่งชี้ถึงบทบาทที่เป็นไปได้ของปัจจัยการเจริญเติบโตนี้ในการเกิดโรคข้อเสื่อม นอกจากนี้ เซลล์กระดูกอ่อนยังผลิต IGF อีกด้วย ในการเพาะเลี้ยงเซลล์ที่คล้ายกระดูกอ่อนที่ได้รับมาจากผู้ป่วยโรคข้อเสื่อม พบว่าระดับ IGF เพิ่มขึ้น ซึ่งจะไปเปลี่ยนแปลงการเผาผลาญของกระดูกอ่อน
TGF-b, IGF, BMP และไซโตไคน์ที่ผลิตโดยออสติโอบลาสต์ในกระดูกใต้กระดูกอ่อนอาจส่งผลต่อการผลิตคอลลาจิเนสและเอนไซม์โปรตีโอไลติกอื่นๆ ในกระดูกอ่อน ซึ่งอาจส่งเสริมการปรับโครงสร้าง/การย่อยสลายเมทริกซ์ของกระดูกอ่อน ยังไม่ชัดเจนว่าออสติโอบลาสต์ใน OA ผลิตปัจจัยกระตุ้นโคโลนีของแมคโครฟาจ (M-CSF - ตัวกระตุ้นการสลายของกระดูก) น้อยกว่าเซลล์ปกติหรือไม่ ผลการศึกษาของ AG Uitterlinden et al. (1997) แสดงให้เห็นว่าตัวรับวิตามินดี ซึ่งแสดงออกโดยออสติโอบลาสต์และควบคุมการแสดงออกของปัจจัยจำนวนหนึ่งที่สังเคราะห์โดยเซลล์เหล่านี้ อาจมีบทบาทบางอย่างในการก่อตัวของออสติโอฟิต ซึ่งอธิบายบทบาทของออสติโอบลาสต์ในการเกิดโรคนี้ได้บางส่วน
โดยคำนึงถึงผลการศึกษาข้างต้น G. Hilal และคณะ (1998), J. Martel-Pelletier และคณะ (1997) เสนอสมมติฐานการทำงานต่อไปนี้เกี่ยวกับความสัมพันธ์ระหว่างการปรับโครงสร้างกระดูกใต้กระดูกอ่อนและกระดูกอ่อนที่เหมาะสมในโรคข้อเสื่อม ในระยะเริ่มต้นหรือระยะขั้นสูงของการเกิดโรคข้อเสื่อม กระบวนการปรับโครงสร้างเนื้อเยื่อกระดูกในกระดูกใต้กระดูกอ่อนจะรุนแรงขึ้น ในเวลาเดียวกัน การโหลดซ้ำๆ จะทำให้เกิดการแตกของกระดูกอ่อนในบริเวณนั้นและ/หรือเกิดความไม่สมดุลในระบบ IGF/IGFBP เนื่องจากการตอบสนองที่ผิดปกติของเซลล์สร้างกระดูกใต้กระดูกอ่อน ซึ่งส่งผลให้เกิดภาวะเส้นโลหิตแข็ง ในทางกลับกัน การเกิดการแตกของกระดูกอ่อนที่เหมาะสมและเกิดความเสียหายต่อเมทริกซ์ของกระดูกอ่อน
ภายใต้สภาวะปกติ ความเสียหายนี้จะได้รับการซ่อมแซมโดยการสังเคราะห์และปล่อย IGF-1 และโปรตีนที่จับกับ IGF ในบริเวณนั้น ซึ่งจะกระตุ้นการสร้าง ECM ของกระดูกอ่อนในข้อ ในขณะเดียวกัน ระบบ GF จะส่งเสริมการเติบโตของเซลล์กระดูกใต้กระดูกอ่อนและการสร้างเมทริกซ์ของกระดูก กิจกรรมการสร้างสารอนาโบลิกของระบบ IGF จะเพิ่มขึ้นในกระดูกใต้กระดูกอ่อนของผู้ป่วยโรคข้อเสื่อม ในขณะที่การกระตุ้นระบบ AP/plasmin (ตัวควบคุมระบบ IGF ในบริเวณนั้น) ในกระดูกอ่อนในข้อจะทำให้เกิดการเปลี่ยนแปลงในบริเวณนั้น ในเซลล์สร้างกระดูกในโรคข้อเสื่อม IGF-1 จะขัดขวางการควบคุม AP โดยพลาสมินด้วยประเภทการตอบรับเชิงบวก ดังนั้นจึงสามารถยับยั้งการปรับโครงสร้างใหม่ในเนื้อเยื่อกระดูก ซึ่งในที่สุดจะนำไปสู่โรคข้อเสื่อม ดังนั้นในเนื้อเยื่อกระดูกและกระดูกอ่อน การเหนี่ยวนำ IGF-1 และโปรตีเอสในบริเวณนั้นทำให้กระดูกอ่อนเสียหาย และทำให้กระดูกใต้กระดูกอ่อนหนาขึ้น ซึ่งส่งผลให้กระดูกอ่อนเสียหายมากขึ้น ความไม่สมดุลระหว่างความเสียหายของกระดูกอ่อนที่เกี่ยวข้องกับโรคกระดูกอ่อนแข็งและความสามารถในการซ่อมแซมทำให้เกิดการเปลี่ยนแปลงอย่างค่อยเป็นค่อยไปใน ECM ของกระดูกอ่อนและการพัฒนาของโรคข้อเสื่อม ตามที่ผู้เขียนกล่าว สมมติฐานนี้ยังอธิบายถึงการดำเนินไปอย่างช้าๆ ของโรคอีกด้วย

