ผู้เชี่ยวชาญทางการแพทย์ของบทความ
สิ่งตีพิมพ์ใหม่
ฮิสโตพลาสมาเป็นสาเหตุของโรคฮิสโตพลาสโมซิส
ตรวจสอบล่าสุด: 04.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
ฮิสโตพลาสโมซิสเป็นโรคติดเชื้อราในทางเดินหายใจที่เกิดขึ้นเองตามธรรมชาติ โดยโรคนี้พบได้เฉพาะในทวีปแอฟริกาเท่านั้น โดยโรคฮิสโตพลาสโมซิสในอเมริกา (H. capsulatum) และในแอฟริกา (H. duboisii) เป็นโรคที่พบได้เฉพาะในทวีปแอฟริกาเท่านั้น โดยโรคฮิสโตพลาสโมซิสในอเมริกาจะพบรอยโรคที่ผิวหนัง เนื้อเยื่อใต้ผิวหนัง และกระดูกในประชากรในชนบท รวมถึงในผู้ที่สัมผัสกับดินและฝุ่น นอกจากมนุษย์แล้ว ลิงบาบูนยังเป็นโรคติดเชื้อราในสภาพธรรมชาติอีกด้วย
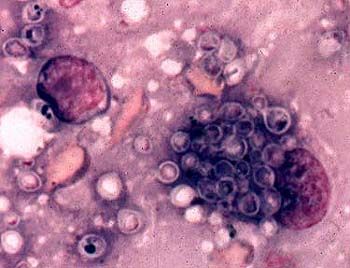
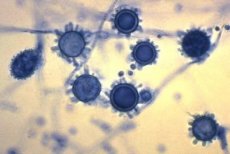
เชื้อที่ทำให้เกิดโรคฮิสโตพลาสโมซิส ได้แก่ Histoplasma capsulatum และ H. duboisii
สัณฐานวิทยาของฮิสโตพลาสมา
เชื้อราที่มีรูปร่างสองแบบระยะไมซีเลียมแสดงด้วยไมซีเลียมมีผนังหนา 1-5 ไมโครโมนิเดียทรงกลมหรือทรงลูกแพร์ เส้นผ่านศูนย์กลาง 1-6 ไมโครโมนิเดียที่มีรูพรุน เส้นผ่านศูนย์กลาง 10-25 ไมโครโมนิเดีย ที่อุณหภูมิ 35-37 องศาเซลเซียส ไมซีเลียมจะเจริญเติบโตเป็นเซลล์ยีสต์ โดยมีขนาด 1.5-2x3-3.5 ไมโครเมตรใน H. capsulatum และ 15-20 ไมโครเมตรใน H. duboisii
คุณสมบัติทางวัฒนธรรมของฮิสโตพลาสมา
เชื้อราที่มีลักษณะคล้ายยีสต์จะมีเนื้อสัมผัสที่นุ่มและมันวาว อุณหภูมิที่เหมาะสมในการเจริญเติบโตคือ 25-30 °C, pH 5.5-6.5 แต่สามารถเจริญเติบโตได้ในช่วง pH กว้างๆ เช่น 5.0-10.0 กิจกรรมทางชีวเคมีอยู่ในระดับต่ำ
โครงสร้างแอนติเจนของฮิสโตพลาสมา
มีแอนติเจนร่วมกับ Blastomyces dermatitidis มีแอนติเจนของยีสต์และเฟสไมซีเลียม (ฮิสโตพลาสมิน) เมื่อเจริญเติบโตในอาหารเหลวเป็นเวลา 3 วัน ไมซีเลียมจะสร้างเอ็กโซแอนติเจน h, m ซึ่งสามารถระบุได้โดยใช้การแพร่กระจายภูมิคุ้มกันในเจล ปัจจัยที่ทำให้เกิดโรค ได้แก่ ไมโครโคนิเดีย ไฮโดรเลส โพลีแซ็กคาไรด์ผนังเซลล์
ช่องนิเวศน์ของฮิสโตพลาสมา
แหล่งที่อยู่อาศัยตามธรรมชาติคือดิน เชื้อราเจริญเติบโตได้ดีในดินที่ปนเปื้อนมูลนกและค้างคาว โดยเชื้อราจะเจริญเติบโตเป็นไมทีเลียม
 [ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ]
[ 12 ], [ 13 ], [ 14 ], [ 15 ], [ 16 ], [ 17 ], [ 18 ], [ 19 ]
นิเวศวิทยา
ยังไม่มีการศึกษา H. duhoisii อย่างเพียงพอ มีรายงานการแยกตัวของสายพันธุ์นี้จากดิน
 [ 20 ], [ 21 ], [ 22 ], [ 23 ]
[ 20 ], [ 21 ], [ 22 ], [ 23 ]
ความยั่งยืนในสิ่งแวดล้อม
ไมโครโคนิเดียมีความต้านทานต่อสภาพแวดล้อมภายนอกได้ดี โดยสามารถดำรงชีวิตอยู่ในดินแห้งได้นานประมาณ 4 ปี และในน้ำที่อุณหภูมิ 4 °C ได้นานประมาณ 600 วัน
ความไวต่อยาปฏิชีวนะ
ไวต่อแอมโฟเทอริซิน บี และคีโตโคนาโซล ไวต่อยาฆ่าเชื้อและน้ำยาฆ่าเชื้อ ไวต่อการทำงานของยาฆ่าเชื้อและน้ำยาฆ่าเชื้อที่ใช้กันทั่วไป
ระบาดวิทยาของโรคฮิสโตพลาสโมซิส
โรคฮิสโตพลาสโมซิส - ซาพรอโนซิส แหล่งที่มาของเชื้อโรคติดต่อในคนและสัตว์คือดินในเขตพื้นที่ที่มีการระบาด พื้นที่ที่มีการระบาด ได้แก่ ทวีปอเมริกาเหนือ ทวีปอเมริกากลาง ทวีปอเมริกาใต้ แคริบเบียน แอฟริกาใต้ อินเดีย เอเชียตะวันออกเฉียงใต้ นิวซีแลนด์ และออสเตรเลีย คนป่วยและสัตว์ไม่สามารถแพร่เชื้อสู่ผู้อื่นได้ กลไกการแพร่เชื้อเป็นแบบอากาศ เส้นทางการแพร่เชื้อคือทางอากาศและฝุ่นละออง ประชากรมีความอ่อนไหวต่อโรคนี้ทั่วไป ในการระบาดของโรค ผู้ป่วยจะสัมผัสกับดิน ยังไม่มีการศึกษาทางระบาดวิทยาของโรคฮิสโตพลาสโมซิสในแอฟริกาอย่างเพียงพอ
อาการของฮิสโตพลาสโมซิส
อาการของโรคฮิสโตพลาสโมซิสขึ้นอยู่กับสถานะภูมิคุ้มกันของสิ่งมีชีวิต โดยจะพบอาการเฉียบพลันในเด็กเนื่องจากระบบภูมิคุ้มกันที่มีลักษณะเฉพาะ ส่วนอาการเรื้อรังที่แพร่กระจายมักเกิดขึ้นจากความไม่เพียงพอของการเชื่อมโยงระหว่างเซลล์กับภูมิคุ้มกัน อาการแสดงของโรคฮิสโตพลาสโมซิสอาจแตกต่างกันไปตั้งแต่การติดเชื้อในปอดเฉียบพลันซึ่งสิ้นสุดลงด้วยการฟื้นตัวโดยธรรมชาติ ไปจนถึงโรคฮิสโตพลาสโมซิสโพรงเรื้อรังและการติดเชื้อลุกลามไปทั่วร่างกาย
การวินิจฉัยทางห้องปฏิบัติการของโรคฮิสโตพลาสโมซิส
วัสดุที่ตรวจพบคือหนองจากแผลหลุมบนผิวหนังและเยื่อเมือก เสมหะ เลือด ปัสสาวะ น้ำไขกระดูก ม้าม ตับ ต่อมน้ำเหลือง และเนื้อเยื่อใต้ผิวหนัง
การวินิจฉัยทางห้องปฏิบัติการจะใช้การตรวจด้วยกล้องจุลทรรศน์ การตรวจทางเชื้อรา การตรวจทางชีววิทยา การตรวจทางซีรัม การตรวจภูมิแพ้ และการตรวจทางเนื้อเยื่อวิทยา การทำงานกับเชื้อก่อโรคจะดำเนินการในห้องปฏิบัติการที่มีการติดเชื้ออันตรายเป็นพิเศษ
การตรวจด้วยกล้องจุลทรรศน์ของหนองและของเหลวที่ไหลออกมาเผยให้เห็นฮิสโตพลาซึมในเซลล์ไฮเปอร์พลาซึมของระบบฟาโกไซต์โมโนนิวเคลียร์ในรูปเซลล์คล้ายยีสต์รูปไข่ขนาด 10-15 ไมโครเมตร ซึ่งอยู่ภายนอกเซลล์หรือภายในโมโนไซต์และแมคโครฟาจ สเมียร์จะถูกย้อมตามวิธี Romanovsky-Giemsa
ในการแยกเชื้อบริสุทธิ์ จะต้องเพาะเชื้อที่ต้องการศึกษาลงในอาหารเลี้ยงเชื้อ Sabouraud ซีรั่มหรือเลือดเจล และให้เชื้อเข้าสู่ตัวอ่อนไก่ด้วย เติมไทอามีนลงในอาหารเลี้ยงเชื้อเพื่อกระตุ้นการเจริญเติบโต และเติมเพนิซิลลินและสเตรปโตมัยซินเพื่อยับยั้งการเจริญเติบโตของแบคทีเรีย เพาะเชื้อบางส่วนที่อุณหภูมิ 22-30 องศาเซลเซียส และบางส่วนที่อุณหภูมิ 37 องศาเซลเซียสเป็นเวลา 3 สัปดาห์ เชื้อที่แยกได้จะถูกระบุโดยลักษณะทางสัณฐานวิทยาและผลของการทดลองทางชีวภาพในหนู การตรวจจับเชื้อราสองเฟสที่มีสัณฐานวิทยาเฉพาะของเฟสไมซีเลียม (ไมซีเลียมมีผนังบาง ไมโครโคนิเดีย และมาโครโคนิเดียวัณโรค) และกลุ่มที่ประกอบด้วยเซลล์ขนาดเล็ก ช่วยให้ระบุ H. capsulation ได้
การแยกเฉพาะเชื้อราที่มีรูปร่างเป็นไมซีเลียมนั้นต้องพิสูจน์ความแตกต่างระหว่างรูปร่างและลักษณะ การเปลี่ยนแปลงทำได้โดยการปลูกไมซีเลียมที่อุณหภูมิ 30-35 องศาเซลเซียส หรือโดยการติดเชื้อในช่องท้องของหนู ซึ่งจะตายภายใน 2-6 สัปดาห์ และตรวจพบยีสต์ขนาดเล็กในอวัยวะภายใน
เชื้อบริสุทธิ์จะถูกแยกออกจากกันโดยการติดเชื้อในช่องท้องของหนูขาวหรือหนูแฮมสเตอร์สีทอง หลังจากนั้นหนึ่งเดือน สัตว์จะถูกฆ่า ตับและม้ามที่ถูกบดจะถูกเพาะในอาหารเลี้ยงเชื้อ Sabouraud ที่มีกลูโคส และเชื้อก่อโรคจะถูกเพาะที่อุณหภูมิ 25, 30 และ 37 องศาเซลเซียสเป็นเวลา 4 สัปดาห์
การแยกเชื้อในฮิสโตพลาสโมซิสขั้นต้นทำได้ยากเนื่องจากมีการเปลี่ยนแปลงเพียงเล็กน้อยในปอด ดังนั้นในกรณีดังกล่าว ควรใช้ผลของปฏิกิริยาทางเซรุ่มวิทยา ซึ่งปฏิกิริยาที่ได้ผลมากที่สุดคือ RP และ RSK โดยฮิสโตพลาสมิน RP การแพร่กระจายภูมิคุ้มกัน และการเกาะกลุ่มลาเท็กซ์มีผลบวกในสัปดาห์ที่ 2-5 หลังการติดเชื้อ ในภายหลัง จะตรวจพบ RSK ที่เป็นบวก โดยไทเตอร์จะเพิ่มขึ้นเมื่อการติดเชื้อขยายวงกว้างขึ้น
การทดสอบอินทรามาลด้วยฮิสโตพลาสมิน (1:100) ให้ผลบวกจะปรากฏในระยะเริ่มต้นของโรคและคงอยู่เป็นเวลาหลายปี มีเพียงการเปลี่ยนแปลงปฏิกิริยาจากเชิงลบเป็นบวกเท่านั้นที่มีคุณค่าในการวินิจฉัย การทดสอบอินทรามาลด้วยฮิสโตพลาสมินสามารถกระตุ้นการสร้างแอนติบอดีได้ ดังนั้นจึงต้องทำหลังจากการศึกษาทางซีรัมวิทยา
สำหรับการตรวจทางเนื้อเยื่อวิทยา การเตรียมส่วนต่างๆ จะถูกย้อมด้วยรีเอเจนต์ชิฟฟ์ แต่วิธีโกโมริ-โกรคอตต์จะให้ผลลัพธ์ที่ชัดเจนที่สุด โดยเซลล์ยีสต์จะถูกย้อมเป็นสีดำหรือสีน้ำตาล สามารถพบเชื้อก่อโรคได้ในไซโทพลาซึมของลิมโฟไซต์ ฮิสทิโอไซต์มีลักษณะเป็นเซลล์เดี่ยวหรือเซลล์แตกหน่อขนาดเล็กที่มีรูปร่างกลม

