สิ่งตีพิมพ์ใหม่
ระบบส่งยาแบบวงจรปิดอาจช่วยปรับปรุงการรักษาด้วยเคมีบำบัดได้
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
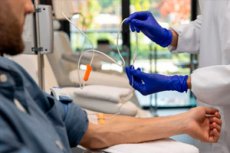
เมื่อผู้ป่วยมะเร็งเข้ารับการทำเคมีบำบัด ปริมาณยาส่วนใหญ่จะคำนวณจากพื้นที่ผิวร่างกายของผู้ป่วย ซึ่งประมาณโดยใช้สมการที่คำนึงถึงส่วนสูงและน้ำหนักของผู้ป่วย สมการนี้ได้รับการคิดค้นขึ้นในปี 1916 โดยอาศัยข้อมูลจากผู้ป่วยเพียง 9 ราย
แนวทางการให้ยาที่เรียบง่ายนี้ไม่ได้คำนึงถึงปัจจัยอื่นๆ และอาจทำให้ผู้ป่วยได้รับยาในปริมาณมากเกินไปหรือไม่เพียงพอ ส่งผลให้ผู้ป่วยบางรายอาจได้รับพิษโดยไม่จำเป็นหรือยาเคมีบำบัดที่ตนได้รับ มีประสิทธิผลไม่เพียงพอ
เพื่อปรับปรุงความแม่นยำของการกำหนดขนาดยาเคมีบำบัด วิศวกรของ MIT ได้พัฒนาวิธีการทางเลือกที่ช่วยให้สามารถกำหนดขนาดยาให้เหมาะกับผู้ป่วยแต่ละคนได้ ระบบของพวกเขาจะวัดปริมาณยาในร่างกายของผู้ป่วยและส่งข้อมูลดังกล่าวไปยังตัวควบคุมที่สามารถปรับอัตราการฉีดยาให้เหมาะสมได้
นักวิจัยกล่าวว่าแนวทางนี้อาจช่วยชดเชยความแตกต่างในเภสัชจลนศาสตร์ของยาที่เกิดจากองค์ประกอบของร่างกาย แนวโน้มทางพันธุกรรม ความเป็นพิษต่ออวัยวะที่เกิดจากเคมีบำบัด ปฏิกิริยากับยาอื่นและอาหาร และการเปลี่ยนแปลงของจังหวะการทำงานของเอนไซม์ที่ทำหน้าที่สลายยาเคมีบำบัดได้
Giovanni Traverso ผู้ช่วยศาสตราจารย์ด้านวิศวกรรมเครื่องกลที่ MIT แพทย์ระบบทางเดินอาหารที่ Brigham and Women's Hospital และผู้เขียนอาวุโสของการศึกษานี้กล่าวว่า "การรับรู้ถึงความก้าวหน้าในการทำความเข้าใจเกี่ยวกับการเผาผลาญยาและการใช้อุปกรณ์ทางวิศวกรรมเพื่อลดความซับซ้อนของการกำหนดขนาดยาเฉพาะบุคคล ทำให้เราเชื่อว่าเราสามารถช่วยเปลี่ยนแปลงความปลอดภัยและประสิทธิภาพของยาหลายชนิดได้"
Louis DeRidder นักศึกษาระดับปริญญาตรีที่ MIT เป็นผู้เขียนหลักของบทความที่ตีพิมพ์ในวารสาร Med
การตรวจสอบอย่างต่อเนื่อง
ในการศึกษานี้ นักวิจัยมุ่งเน้นไปที่ยาที่เรียกว่า5-fluorouracilซึ่งใช้ในการรักษามะเร็งลำไส้ใหญ่และมะเร็งชนิดอื่นๆ โดยทั่วไปยานี้จะได้รับการบริหารเป็นเวลา 46 ชั่วโมง และขนาดยาจะถูกกำหนดโดยใช้สูตรที่อิงตามส่วนสูงและน้ำหนักของผู้ป่วย ซึ่งให้การประมาณพื้นที่ผิวของร่างกาย
อย่างไรก็ตาม แนวทางนี้ไม่ได้คำนึงถึงความแตกต่างในองค์ประกอบของร่างกายที่อาจส่งผลต่อการกระจายตัวของยาในร่างกาย หรือการเปลี่ยนแปลงทางพันธุกรรมที่ส่งผลต่อการเผาผลาญยา ความแตกต่างเหล่านี้อาจนำไปสู่ผลข้างเคียงที่เป็นอันตรายได้หากได้รับยาในปริมาณมากเกินไป หากได้รับยาไม่เพียงพอ อาจทำให้เนื้องอกไม่สามารถฆ่าได้ดังที่คาดไว้
“คนที่มีพื้นที่ผิวร่างกายเท่ากันอาจมีส่วนสูงและน้ำหนักต่างกันมาก มีมวลกล้ามเนื้อต่างกัน หรือมีพันธุกรรมต่างกัน แต่ตราบใดที่ส่วนสูงและน้ำหนักที่แทนลงในสมการนั้นได้พื้นที่ผิวร่างกายเท่ากัน ปริมาณยาที่ใช้ก็จะเท่ากัน” DeRidder นักศึกษาปริญญาเอกสาขาวิศวกรรมการแพทย์และฟิสิกส์การแพทย์จากโครงการวิทยาศาสตร์สุขภาพและเทคโนโลยี Harvard-MIT กล่าว
ปัจจัยอีกประการหนึ่งที่สามารถเปลี่ยนแปลงปริมาณยาในเลือดในช่วงเวลาใดเวลาหนึ่งได้คือความแปรปรวนของจังหวะชีวภาพในเอนไซม์ที่เรียกว่า dihydropyrimidine dehydrogenase (DPD) ซึ่งทำหน้าที่สลาย 5-fluorouracil การแสดงออกของ DPD เช่นเดียวกับเอนไซม์อื่นๆ ในร่างกาย จะถูกควบคุมโดยจังหวะชีวภาพ ดังนั้น การย่อยสลาย 5-FU โดย DPD จึงไม่คงที่ แต่จะแตกต่างกันไปตามช่วงเวลาของวัน จังหวะชีวภาพเหล่านี้อาจทำให้ปริมาณ 5-FU ในเลือดของผู้ป่วยเปลี่ยนแปลงไปสิบเท่าในระหว่างการให้ยา
“การใช้พื้นที่ผิวร่างกายในการคำนวณขนาดยาเคมีบำบัดทำให้เราทราบว่าผู้ป่วย 2 คนอาจมีพิษจาก 5-ฟลูออโรยูราซิลแตกต่างกันมาก ผู้ป่วยรายหนึ่งอาจได้รับการรักษาด้วยยาพิษเพียงเล็กน้อย จากนั้นจึงเข้ารับการรักษาด้วยยาพิษร้ายแรงอีกครั้ง วิธีการเผาผลาญยาเคมีบำบัดของผู้ป่วยในแต่ละรอบเปลี่ยนไป วิธีการให้ยาที่ล้าสมัยของเราไม่ได้บันทึกการเปลี่ยนแปลงเหล่านี้ไว้ และผู้ป่วยต้องทนทุกข์ทรมานจากเหตุการณ์นี้” ดักลาส รูบินสัน แพทย์ผู้เชี่ยวชาญด้านมะเร็งวิทยาจากสถาบันมะเร็งดานา-ฟาร์เบอร์และผู้เขียนรายงานกล่าว
วิธีหนึ่งในการพยายามชดเชยความแปรปรวนในเภสัชจลนศาสตร์ของเคมีบำบัดคือกลยุทธ์ที่เรียกว่าการติดตามยารักษา ซึ่งผู้ป่วยจะให้ตัวอย่างเลือดในตอนท้ายของรอบการรักษาหนึ่งรอบ หลังจากวิเคราะห์ตัวอย่างนี้เพื่อดูความเข้มข้นของยาแล้ว หากจำเป็น สามารถปรับขนาดยาได้ในช่วงต้นของรอบการรักษารอบต่อไป (โดยปกติคือสองสัปดาห์สำหรับ 5-ฟลูออโรยูราซิล)
แนวทางนี้ได้รับการพิสูจน์แล้วว่าให้ผลลัพธ์ที่ดีขึ้นสำหรับผู้ป่วย แต่ยังไม่ได้ถูกใช้กันอย่างแพร่หลายสำหรับเคมีบำบัด เช่น 5-ฟลูออโรยูราซิล
นักวิจัย MIT ต้องการพัฒนาวิธีการตรวจติดตามประเภทเดียวกัน แต่จะต้องเป็นระบบอัตโนมัติ ซึ่งจะช่วยให้สามารถกำหนดขนาดยาได้แบบเรียลไทม์ ซึ่งอาจนำไปสู่ผลลัพธ์ที่ดีกว่าสำหรับผู้ป่วยได้
ในระบบวงจรปิด ความเข้มข้นของยาสามารถตรวจสอบได้อย่างต่อเนื่อง และข้อมูลนี้จะถูกใช้เพื่อปรับอัตราการฉีดยาเคมีบำบัดโดยอัตโนมัติเพื่อรักษาปริมาณยาให้อยู่ในช่วงเป้าหมาย
ระบบวงจรปิดนี้ช่วยให้สามารถกำหนดขนาดยาได้ตามจังหวะชีวภาพของระดับเอนไซม์ที่เผาผลาญยา รวมถึงการเปลี่ยนแปลงใดๆ ในด้านเภสัชจลนศาสตร์ของผู้ป่วยนับตั้งแต่การรักษาครั้งสุดท้าย เช่น ความเป็นพิษต่ออวัยวะที่เกิดจากเคมีบำบัด
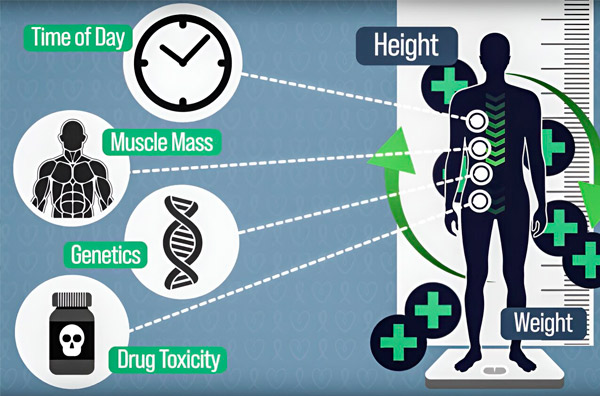
เพื่อให้การกำหนดขนาดยาเคมีบำบัดแม่นยำยิ่งขึ้น วิศวกรจากสถาบันเทคโนโลยีแมสซาชูเซตส์ได้พัฒนาวิธีการวัดปริมาณยาในร่างกายของผู้ป่วยอย่างต่อเนื่องตลอดระยะเวลาการให้ยาหลายชั่วโมง ซึ่งจะช่วยชดเชยความแตกต่างที่เกิดจากองค์ประกอบของร่างกาย พันธุกรรม ความเป็นพิษของยา และจังหวะการเต้นของนาฬิกาชีวภาพ แหล่งที่มา: ขอขอบคุณนักวิจัย
ระบบใหม่ที่พัฒนาโดยนักวิจัย ซึ่งเรียกว่า CLAUDIA (Closed-Loop AUtomated Drug Infusion regulAtor) ใช้เครื่องมือที่มีจำหน่ายในเชิงพาณิชย์ในแต่ละขั้นตอน โดยจะเก็บตัวอย่างเลือดทุก ๆ ห้านาที และเตรียมให้พร้อมสำหรับการวิเคราะห์อย่างรวดเร็ว วัดความเข้มข้นของ 5-ฟลูออโรยูราซิลในเลือดและเปรียบเทียบกับช่วงเป้าหมาย
ความแตกต่างระหว่างเป้าหมายและความเข้มข้นที่วัดได้จะถูกป้อนเข้าสู่อัลกอริทึมการควบคุม ซึ่งจากนั้นจะปรับอัตราการแช่ตามความจำเป็นเพื่อรักษาขนาดยาให้อยู่ในช่วงความเข้มข้นที่ยาจะมีประสิทธิผลและไม่มีพิษ
“เราได้พัฒนาระบบที่เราสามารถวัดความเข้มข้นของยาได้อย่างต่อเนื่อง และปรับอัตราการฉีดให้เหมาะสมเพื่อรักษาความเข้มข้นของยาในช่วงเวลาการรักษา” DeRidder กล่าว
ปรับแต่งอย่างรวดเร็ว
ในการทดลองกับสัตว์ นักวิจัยพบว่าการใช้ CLAUDIA ช่วยให้สามารถควบคุมปริมาณยาที่หมุนเวียนในร่างกายให้อยู่ในช่วงเป้าหมายได้ประมาณร้อยละ 45 ของเวลา
ระดับยาในสัตว์ที่ได้รับเคมีบำบัดโดยไม่ได้รับคลอเดียยังคงอยู่ในช่วงเป้าหมายเพียงร้อยละ 13 ของเวลาโดยเฉลี่ย นักวิจัยไม่ได้ทดสอบประสิทธิภาพของระดับยาในการศึกษานี้ แต่การรักษาความเข้มข้นในช่วงเป้าหมายเชื่อว่าจะส่งผลให้ผลลัพธ์ดีขึ้นและเกิดพิษน้อยลง
นอกจากนี้ CLAUDIA ยังสามารถรักษาปริมาณ 5-fluorouracil ให้อยู่ในช่วงเป้าหมายได้ แม้ว่าจะใช้ยาที่ยับยั้งเอนไซม์ DPD ก็ตาม ในสัตว์ที่ได้รับสารยับยั้งนี้โดยไม่ได้ติดตามและปรับปริมาณอย่างต่อเนื่อง ระดับ 5-fluorouracil จะเพิ่มขึ้นถึงแปดเท่า
สำหรับการสาธิตนี้ นักวิจัยดำเนินการแต่ละขั้นตอนของกระบวนการด้วยตนเองโดยใช้อุปกรณ์สำเร็จรูป แต่ปัจจุบันมีแผนที่จะทำให้แต่ละขั้นตอนเป็นอัตโนมัติ เพื่อให้สามารถตรวจสอบและปรับขนาดยาได้โดยไม่ต้องมีการแทรกแซงจากมนุษย์
ในการวัดความเข้มข้นของยา นักวิจัยได้ใช้เครื่องโครมาโทกราฟีของเหลวสมรรถนะสูง-แมสสเปกโตรเมตรี (HPLC-MS) ซึ่งเป็นเทคนิคที่สามารถปรับใช้ในการตรวจจับยาเกือบทุกประเภทได้
“เราเห็นอนาคตที่เราสามารถใช้ CLAUDIA สำหรับยาใดๆ ก็ได้ที่มีคุณสมบัติทางเภสัชจลนศาสตร์ที่เหมาะสม และสามารถตรวจจับได้ด้วย HPLC-MS ช่วยให้สามารถกำหนดปริมาณยาที่เหมาะกับแต่ละบุคคลสำหรับยาต่างๆ หลายชนิดได้” DeRidder กล่าว
