สิ่งตีพิมพ์ใหม่
กลไกทางพันธุกรรมแบบใหม่นี้อาจให้เป้าหมายการรักษาต่อเนื้องอกในสมองได้
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
ผลการศึกษาวิจัยจากห้องปฏิบัติการของศาสตราจารย์ Shi-Yuan Cheng, PhD จากแผนกประสาทวิทยา Ken and Ruth Davey ในภาควิชาประสาทวิทยา ได้ระบุกลไกใหม่ที่เป็นพื้นฐานของเหตุการณ์การตัดต่อ RNA ทางเลือกในเซลล์เนื้องอกในสมองซึ่งอาจใช้เป็นเป้าหมายการรักษาใหม่ได้ ผลการศึกษาวิจัยดังกล่าวได้รับการตีพิมพ์ในวารสาร Journal of Clinical Investigation
“เราพบวิธีการรักษาเนื้องอกในสมอง ที่แตกต่างออก ไปโดยใช้วิธีการตัดต่อทางเลือก และค้นพบเป้าหมายใหม่ที่ยังไม่เคยระบุมาก่อน แต่มีความสำคัญต่อมะเร็งเนื้องอกในสมอง” ดร. เสี่ยว ซ่ง ผู้ช่วยศาสตราจารย์ด้านประสาทวิทยาและผู้เขียนหลักของการศึกษากล่าว
เนื้องอกในสมองชนิด Gliomas เป็นเนื้องอกในสมองชนิดที่พบบ่อยที่สุดในผู้ใหญ่ โดยมีต้นกำเนิดมาจากเซลล์เกลีย ซึ่งอยู่ในระบบประสาทส่วนกลางและทำหน้าที่รองรับเซลล์ประสาทข้างเคียง เนื้องอกในสมองชนิด Gliomas มีความต้านทานต่อการรักษาแบบมาตรฐานสูง รวมถึงการฉายรังสีและเคมีบำบัดเนื่องจากเนื้องอกชนิดนี้มีความผิดปกติทางพันธุกรรมและเอพิเจเนติกส์ จึงทำให้จำเป็นต้องค้นหาเป้าหมายการรักษาใหม่ๆ
งานวิจัยก่อนหน้านี้จากห้องปฏิบัติการ Cheng ที่ตีพิมพ์ในวารสาร Cancer Researchแสดงให้เห็นว่าปัจจัยการตัดต่อที่สำคัญ SRSF3 เพิ่มขึ้นอย่างมีนัยสำคัญในก้อนเนื้อในสมองเมื่อเทียบกับสมองปกติ และการตัดต่อ RNA ที่ควบคุมโดย SRSF3 จะส่งเสริมการเจริญเติบโตและความก้าวหน้าของก้อนเนื้อในสมองด้วยการมีอิทธิพลต่อกระบวนการเซลล์หลายเซลล์ในเซลล์เนื้องอก
การต่อกันของ RNA เป็นกระบวนการที่เกี่ยวข้องกับการกำจัดอินทรอน (บริเวณที่ไม่เข้ารหัสของ RNA) และการรวมกันของเอ็กซอน (บริเวณเข้ารหัส) เพื่อสร้างโมเลกุล mRNA ที่โตเต็มที่ซึ่งสนับสนุนการแสดงออกของยีนในเซลล์
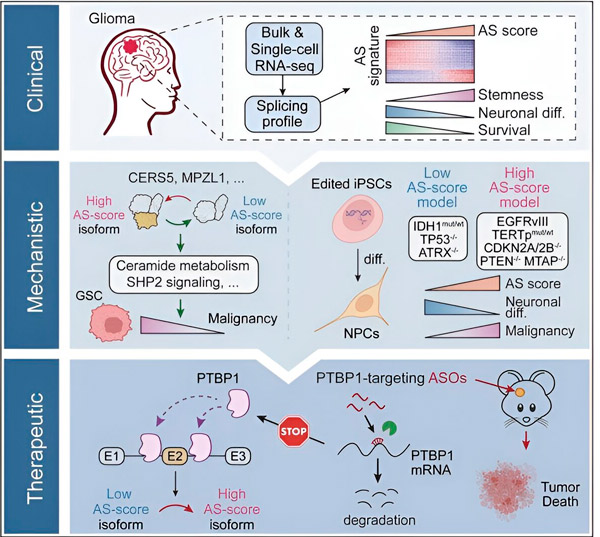
ในการศึกษานี้ นักวิทยาศาสตร์มุ่งหวังที่จะระบุการเปลี่ยนแปลงในการตัดต่อทางเลือกในเซลล์เนื้องอกกาวเนื้อสมอง กลไกที่อยู่เบื้องหลังการเปลี่ยนแปลงเหล่านี้ และกำหนดศักยภาพของการเปลี่ยนแปลงเหล่านี้ในฐานะเป้าหมายการรักษา
นักวิจัยใช้การคำนวณและเทคโนโลยีการจัดลำดับอาร์เอ็นเอเพื่อศึกษาการเปลี่ยนแปลงของการตัดต่อในเซลล์เนื้องอกในสมองจากตัวอย่างผู้ป่วย เพื่อยืนยันการเปลี่ยนแปลงเหล่านี้ พวกเขาใช้เทคโนโลยีการตัดต่อยีน CRISPR เพื่อนำการกลายพันธุ์ของไดรเวอร์ในเนื้องอกในสมองที่แตกต่างกันเข้าไปในโมเดลเนื้องอกในสมองที่ได้มาจากเซลล์ต้นกำเนิดพลูริโพเทนต์ที่เหนี่ยวนำโดยมนุษย์ (iPSC)
พวกเขาพบว่าการเปลี่ยนแปลงการตัดต่อนี้ได้รับการส่งเสริมโดยตัวรับปัจจัยการเจริญเติบโตของหนังกำพร้า III (EGFRIII) ซึ่งเป็นที่รู้กันว่ามีการแสดงออกมากเกินไปในเนื้องอกหลายชนิด รวมทั้งก้อนเนื้อในสมอง และถูกยับยั้งโดยการกลายพันธุ์ของยีน IDH1
นักวิจัยได้ยืนยันการทำงานของเหตุการณ์การตัดต่อ RNA สองเหตุการณ์ที่สร้างโปรตีนไอโซฟอร์มที่แตกต่างกันโดยมีลำดับกรดอะมิโนที่แตกต่างกัน
“มีเพียงไอโซฟอร์มเดียวเท่านั้นที่สามารถส่งเสริมการเติบโตของเนื้องอก ซึ่งแตกต่างจากไอโซฟอร์มอีกแบบหนึ่งที่ปกติแล้วจะแสดงออกมาในสมองปกติ เนื้องอกใช้ประโยชน์จากกลไกนี้เพื่อแสดงไอโซฟอร์มที่ส่งเสริมการเติบโตของเนื้องอกอย่างเลือกสรรมากกว่าไอโซฟอร์มสมองปกติ” ซองกล่าว
จากนั้นทีมวิจัยได้วิเคราะห์โปรตีนที่จับกับ RNA ต้นน้ำและพบว่ายีน PTBP1 ควบคุมการตัดต่อ RNA ที่ส่งเสริมเนื้องอกในเซลล์กีลีโอม่า โดยใช้แบบจำลองกีลีโอม่าออร์โธโทปิกในหนูที่มีภูมิคุ้มกันบกพร่อง นักวิจัยได้กำหนดเป้าหมาย PTBP1 ด้วยการบำบัดโดยใช้โอลิโกนิวคลีโอไทด์แอนติเซนส์ (ASO) ซึ่งสุดท้ายแล้วสามารถยับยั้งการเติบโตของเนื้องอกได้
“ข้อมูลของเราเน้นย้ำถึงบทบาทของการตัดต่อ RNA ทางเลือกในการมีอิทธิพลต่อมะเร็งกาวเนื้อสมองและความไม่เหมือนกัน และศักยภาพในการเป็นช่องโหว่ทางการรักษาสำหรับการรักษากาวเนื้อสมองในผู้ใหญ่” ผู้เขียนผลการศึกษากล่าว
ขั้นตอนต่อไปสำหรับนักวิจัยคือการสำรวจศักยภาพในการกำหนดเป้าหมาย PTBP1 เพื่อกระตุ้นการตอบสนองทางภูมิคุ้มกันต่อต้านเนื้องอก ซ่งกล่าว
“จากการวิเคราะห์การจัดลำดับ RNA แบบอ่านยาว เราพบว่าการกำหนดเป้าหมาย PTBP1 ในเซลล์กาวเนื้อสมองส่งผลให้เกิดการสร้างทรานสคริปต์ที่ตัดต่อทางเลือกหลายรายการซึ่งไม่มีอยู่ในเนื้อเยื่อปกติ ดังนั้น โครงการต่อไปของเราคือการค้นหาว่าไอโซฟอร์มนี้สามารถสร้างแอนติเจนบางชนิดได้หรือไม่ เพื่อให้ระบบภูมิคุ้มกันสามารถจดจำเนื้องอกได้ดีขึ้น” ซองกล่าว
นอกจากนี้ Song ยังกล่าวเสริมด้วยว่าทีมงานของพวกเขามีความสนใจในการวิเคราะห์การเปลี่ยนแปลงการตัดต่อในเซลล์ที่ไม่ใช่เนื้องอกจากผู้ป่วยมะเร็งกาวเนื้อสมอง เช่น เซลล์ภูมิคุ้มกัน
“เราทราบอยู่แล้วว่าการตัดต่อมีความสำคัญมากในการควบคุมการทำงานในเซลล์ ดังนั้น การตัดต่อจึงไม่เพียงแต่ควบคุมความร้ายแรงของเนื้องอกเท่านั้น แต่ยังสามารถควบคุมการทำงานของเซลล์ภูมิคุ้มกันได้ด้วย เพื่อตรวจสอบว่าเซลล์ภูมิคุ้มกันสามารถฆ่ามะเร็งได้อย่างมีประสิทธิภาพหรือไม่ ดังนั้น เราจึงกำลังทำการวิเคราะห์ชีวสารสนเทศในเซลล์ภูมิคุ้มกันที่แทรกซึมเข้าไปในเนื้องอก เพื่อดูว่ามีการเปลี่ยนแปลงในการตัดต่อหรือไม่หลังจากที่เซลล์ภูมิคุ้มกันแทรกซึมเข้าไปในเนื้องอก
“เป้าหมายของเราคือการพิจารณาบทบาทของการตัดต่อทางเลือกในการกำหนดรูปร่างของสภาพแวดล้อมของเนื้องอกที่กดภูมิคุ้มกันและระบุเป้าหมายที่มีศักยภาพในการปรับปรุงประสิทธิภาพของภูมิคุ้มกันบำบัดในมะเร็งกาวเนื้อสมอง” ซองกล่าว
