อนุพันธ์ของธาลิโดไมด์นำไปสู่การตายของเซลล์มะเร็งที่ดื้อยา
ตรวจสอบล่าสุด: 14.06.2024

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
การศึกษาที่ดำเนินการโดยมหาวิทยาลัยเกอเธ่ แฟรงก์เฟิร์ต ชี้ให้เห็นความเป็นไปได้ที่อนุพันธ์ของทาลิโดไมด์มีศักยภาพในการรักษาโรคมะเร็ง ในช่วงทศวรรษปี 1950 มีการขายทาลิโดไมด์เป็นยานอนหลับ ต่อมามีชื่อเสียงในเรื่องการทำให้เกิดความผิดปกติร้ายแรงในทารกในครรภ์ในระยะแรกของการตั้งครรภ์
เป็นที่รู้กันว่าโมเลกุลทำหน้าที่ทำเครื่องหมายโปรตีนในเซลล์เพื่อการทำลาย ในการวิจัยในปัจจุบัน นักวิทยาศาสตร์ได้สร้างอนุพันธ์ของทาลิโดไมด์ พวกเขาสามารถแสดงให้เห็นว่าสารเหล่านี้ส่งผลต่อการทำลายโปรตีนที่รับผิดชอบต่อความอยู่รอดของเซลล์มะเร็ง
บางทีอาจจะไม่มีโมเลกุลอื่นใดที่มีอดีตอันปั่นป่วนเช่นทาลิโดไมด์ มันเป็นส่วนประกอบหลักของยาที่ได้รับการอนุมัติในหลายประเทศในช่วงทศวรรษ 1950 ว่าเป็นยาระงับประสาทและถูกสะกดจิต อย่างไรก็ตาม ในไม่ช้าก็เห็นได้ชัดว่าหญิงตั้งครรภ์ที่รับประทานทาลิโดไมด์มักให้กำเนิดเด็กที่มีความผิดปกติร้ายแรง
อย่างไรก็ตาม ในช่วงไม่กี่ทศวรรษที่ผ่านมา ยาได้ตั้งความหวังไว้สูงอีกครั้ง การวิจัยแสดงให้เห็นว่า ยับยั้งการเจริญเติบโตของหลอดเลือด ดังนั้นจึงอาจเหมาะสมที่จะตัดเนื้องอกออกจากสารอาหารของมัน จากนั้น ยังได้รับการพิสูจน์แล้วว่ามีประสิทธิภาพมากในการรักษามัลติเพิล มัยอิโลมา ซึ่งเป็นเนื้องอกเนื้อร้ายในไขกระดูก
“ตอนนี้เรารู้แล้วว่าทาลิโดไมด์สามารถเรียกได้ว่าเป็น 'กาวโมเลกุล'” ดร. Xinglai Cheng จากสถาบันเภสัชเคมี มหาวิทยาลัยเกอเธ่ แฟรงก์เฟิร์ต อธิบาย "ซึ่งหมายความว่ามันสามารถจับโปรตีนสองตัวมารวมกันได้"
สิ่งนี้น่าสนใจเป็นพิเศษเพราะหนึ่งในโปรตีนเหล่านี้เป็น "เครื่องติดฉลาก" โดยติดฉลาก "ถังขยะ" ที่ไม่คลุมเครือไว้กับโปรตีนอีกชนิดหนึ่ง
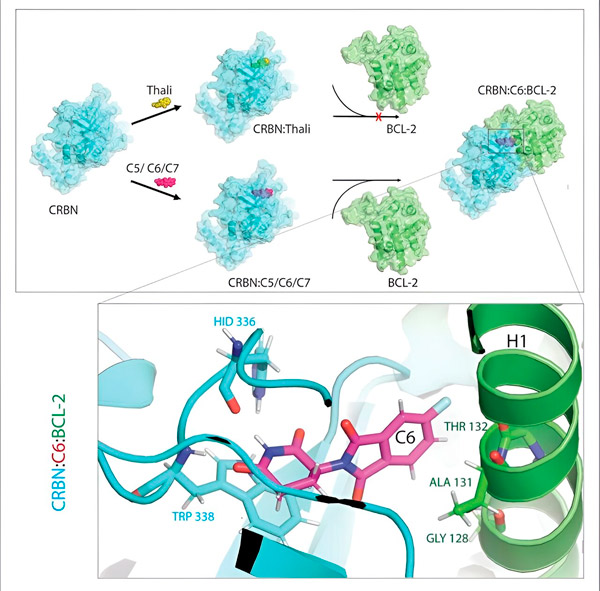
อนุพันธ์ธาลิโดไมด์ C5, C6 และ C7 ดัดแปลง CRBN ซึ่งเป็น "เครื่องติดฉลาก" เพื่อให้สามารถจับกับ BCL-2 ได้ ดังนั้นโมเลกุล BCL-2 จึงถูกทำเครื่องหมายสำหรับการย่อยสลาย ซึ่งเป็นกลยุทธ์ใหม่ที่เป็นไปได้ในการต่อสู้กับโรคมะเร็ง ผู้แต่ง: ดร.ซิงไหล เฉิง
ระบบกำจัดของเสียของเซลล์จดจำแท็กนี้ได้ โดยจะจับโมเลกุลโปรตีนที่มีข้อความกำกับไว้แล้วฉีกเป็นชิ้นเล็กชิ้นน้อย "กลไกนี้เองที่อธิบายผลต่างๆ ของธาลิโดไมด์" เฉิงกล่าว "สิ่งนี้สามารถนำไปสู่ความผิดปกติในระหว่างการพัฒนาของตัวอ่อนหรือการทำลายเซลล์มะเร็ง ทั้งนี้ขึ้นอยู่กับว่าโปรตีนชนิดใดถูกติดแท็ก"
กลไกนี้ให้ผลทางการแพทย์ที่ดีเยี่ยม เนื่องจากเซลล์มะเร็งต้องอาศัยโปรตีนบางชนิดเพื่อความอยู่รอด หากสามารถกำหนดเป้าหมายและทำลายอย่างเป็นระบบ โรคนี้ก็อาจหายขาดได้ ปัญหาคือกาวโมเลกุลค่อนข้างแปลก
พันธมิตรที่มีผลผูกพันรายหนึ่งมักจะเป็นเครื่องทำเครื่องหมายเซลล์ หรือในสำนวนทางวิทยาศาสตร์ นั่นคือ E3 ligase ที่เรียกว่า CRBN มีโปรตีนเพียงไม่กี่ตัวจากหลายพันโปรตีนในร่างกายที่สามารถเป็นคู่ที่สองได้ ซึ่งโปรตีนเหล่านี้ขึ้นอยู่กับกาว
"ดังนั้นเราจึงสร้างอนุพันธ์ของธาลิโดไมด์ขึ้นมา" เฉิงกล่าว "จากนั้นเราตรวจสอบว่าพวกมันมีคุณสมบัติในการยึดเกาะหรือไม่ และถ้าเป็นเช่นนั้น พวกมันมีฤทธิ์ต้านโปรตีนชนิดใด" เมื่อต้องการทำเช่นนี้ นักวิจัยได้เพิ่มอนุพันธ์ของพวกมันลงในโปรตีนทั้งหมดในเซลล์ที่โตแล้ว จากนั้น พวกเขาสังเกตว่าโปรตีนใดต่อไปนี้สลายตัวเมื่อมี CRBN
"ในกระบวนการนี้ เราได้ระบุอนุพันธ์สามชนิดที่สามารถแท็กโปรตีนในเซลล์ซึ่งมีความสำคัญมากต่อการย่อยสลาย นั่นคือ BCL-2" Cheng อธิบาย "BCL-2 ป้องกันไม่ให้เซลล์เปิดใช้งานโปรแกรมการทำลายตนเอง ดังนั้นหากขาดหายไป เซลล์ก็จะตาย"
BCL-2 จึงเป็นจุดสนใจของการวิจัยโรคมะเร็งมายาวนาน มีแม้กระทั่งยาสำหรับโรคมะเร็งเม็ดเลือดขาวที่เรียกว่า venetoclax อยู่แล้ว ซึ่งลดประสิทธิภาพของ BCL-2 และทำให้เซลล์ที่กลายพันธุ์ทำลายตัวเอง
"อย่างไรก็ตาม ในเซลล์มะเร็งจำนวนมาก BCL-2 เองก็กลายพันธุ์ไป ดังนั้น venetoclax จึงไม่ยับยั้งโปรตีนอีกต่อไป" เฉิงกล่าว "เราสามารถแสดงให้เห็นว่าอนุพันธ์ของเรายังระบุรูปแบบการย่อยสลายที่กลายพันธุ์นี้อีกด้วย นอกจากนี้ พันธมิตรของเราที่ Max Planck Institute for Biophysics ยังได้จำลองอันตรกิริยาของอนุพันธ์ธาลิโดไมด์กับ BCL-2 บนคอมพิวเตอร์ ซึ่งแสดงให้เห็นว่าอนุพันธ์จับกับ ตำแหน่งที่แตกต่างจากเวเนโทแคล็กซ์อย่างสิ้นเชิง ซึ่งเป็นผลลัพธ์ที่เราสามารถยืนยันได้จากการทดลองในภายหลัง"
นอกจากนี้ นักวิจัยได้ทดสอบสารของพวกเขากับแมลงวันผลไม้ที่มีเซลล์มะเร็ง อัตราการรอดชีวิตของแมลงวันที่ได้รับการบำบัดด้วยวิธีนี้สูงขึ้นอย่างมีนัยสำคัญ อย่างไรก็ตาม เฉิงเตือนอย่าตื่นเต้นเกินไป เพราะผลลัพธ์เหล่านี้ยังคงเป็นงานวิจัยพื้นฐาน "แม้ว่าพวกมันจะแสดงให้เห็นว่าโมเลกุลทาลิโดไมด์ที่ได้รับการดัดแปลงมีศักยภาพในการรักษาที่ดีเยี่ยม แต่เรายังไม่สามารถบอกได้ว่าพวกมันจะพิสูจน์ตัวเองในทางปฏิบัติ ณ จุดใดเวลาหนึ่งได้หรือไม่"
ผลการศึกษาได้รับการตีพิมพ์ใน วารสาร Cell Reports Physical Science
