สิ่งตีพิมพ์ใหม่
การกลายพันธุ์ของยีน ARID1A ทำให้เนื้องอกไวต่อภูมิคุ้มกันบำบัด
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
ในช่วงไม่กี่ปีที่ผ่านมา ภูมิคุ้มกันบำบัดได้ปฏิวัติการรักษามะเร็ง แทนที่จะกำหนดเป้าหมายที่เนื้องอกโดยตรง ภูมิคุ้มกันบำบัดจะสั่งให้ระบบภูมิคุ้มกันของผู้ป่วยโจมตีเนื้องอกอย่างมีประสิทธิภาพมากขึ้น วิธีนี้ได้ผลดีโดยเฉพาะกับมะเร็งบางชนิดที่รักษายาก อย่างไรก็ตาม ผู้ป่วยมะเร็งน้อยกว่าครึ่งหนึ่งตอบสนองต่อภูมิคุ้มกันบำบัดในปัจจุบัน ทำให้เกิดความจำเป็นเร่งด่วนในการระบุไบโอมาร์กเกอร์ที่สามารถทำนายได้ว่าผู้ป่วยรายใดมีแนวโน้มที่จะได้รับประโยชน์สูงสุดจากการรักษา
เมื่อไม่นานมานี้ นักวิทยาศาสตร์ได้สังเกตเห็นว่าผู้ป่วยที่มีเนื้องอกมีการกลายพันธุ์ในยีน ARID1A มีแนวโน้มที่จะตอบสนองต่อการปิดกั้นจุดตรวจภูมิคุ้มกันเป็นบวกมากขึ้น ซึ่ง เป็นวิธีบำบัด ภูมิคุ้มกัน ประเภทหนึ่ง ที่ออกฤทธิ์โดยทำให้เซลล์ภูมิคุ้มกันที่ต่อสู้กับมะเร็งทำงานอย่างปกติ
เนื่องจากการกลายพันธุ์ของยีน ARID1A มีอยู่ในมะเร็งหลายชนิด รวมถึงมะเร็งเยื่อบุโพรงมดลูก มะเร็งรังไข่ มะเร็งลำไส้ใหญ่และทวารหนัก มะเร็งกระเพาะอาหาร มะเร็งตับ และมะเร็งตับอ่อน นักวิจัยของสถาบัน Salk จึงสงสัยว่าการกลายพันธุ์นี้จะส่งผลต่อความไวต่อการรักษาได้อย่างไร และแพทย์จะใช้ข้อมูลนี้เพื่อปรับการรักษามะเร็งเฉพาะบุคคลสำหรับผู้ป่วยแต่ละรายได้อย่างไร
การศึกษาใหม่ของพวกเขาที่ตีพิมพ์ในวารสาร Cellแสดงให้เห็นว่าการกลายพันธุ์ ARID1A ทำให้เนื้องอกไวต่อภูมิคุ้มกันบำบัดด้วยการคัดเลือกเซลล์ภูมิคุ้มกันที่ต่อสู้กับมะเร็งไปที่เนื้องอกผ่านการตอบสนองทางภูมิคุ้มกันแบบต่อต้านไวรัส
นักวิจัยแนะนำว่าการกลายพันธุ์และการตอบสนองภูมิคุ้มกันต่อต้านไวรัสนี้อาจใช้เป็นไบโอมาร์กเกอร์เพื่อคัดเลือกผู้ป่วยสำหรับภูมิคุ้มกันบำบัดเฉพาะ เช่น การปิดกั้นจุดตรวจภูมิคุ้มกันได้ดีขึ้น ผลการค้นพบเหล่านี้ยังสนับสนุนการพัฒนายาที่กำหนดเป้าหมายไปที่ ARID1A และโปรตีนที่เกี่ยวข้องเพื่อให้เนื้องอกอื่นไวต่อภูมิคุ้มกันบำบัดมากขึ้น
“สิ่งนี้อาจเปลี่ยนผลลัพธ์ของการรักษามะเร็งสำหรับผู้ป่วยได้จริง” รองศาสตราจารย์ไดอานา ฮาร์เกรฟส์ ผู้เขียนอาวุโสของการศึกษากล่าว “ผู้ป่วยที่มีการกลายพันธุ์ของ ARID1A มีการตอบสนองทางภูมิคุ้มกันอยู่แล้ว ดังนั้น สิ่งที่เราต้องทำคือกระตุ้นการตอบสนองนั้นด้วยการปิดกั้นจุดตรวจภูมิคุ้มกันเพื่อช่วยให้พวกเขาทำลายเนื้องอกจากภายใน”
แม้ว่าจะทราบกันดีว่าผู้ที่มีการกลายพันธุ์ของ ARID1A ตอบสนองต่อการปิดกั้นจุดตรวจภูมิคุ้มกันได้ดี แต่ความเชื่อมโยงที่ชัดเจนระหว่างทั้งสองอย่างยังคงไม่ชัดเจน นักวิทยาศาสตร์จากสถาบัน Salk ได้ใช้เมาส์จำลองมะเร็งผิวหนังเมลาโนมาและมะเร็งลำไส้ใหญ่ที่มีทั้งการกลายพันธุ์ของ ARID1A และ ARID1A ที่ทำหน้าที่ได้ เพื่อไขความกระจ่างเกี่ยวกับกลไกดังกล่าว
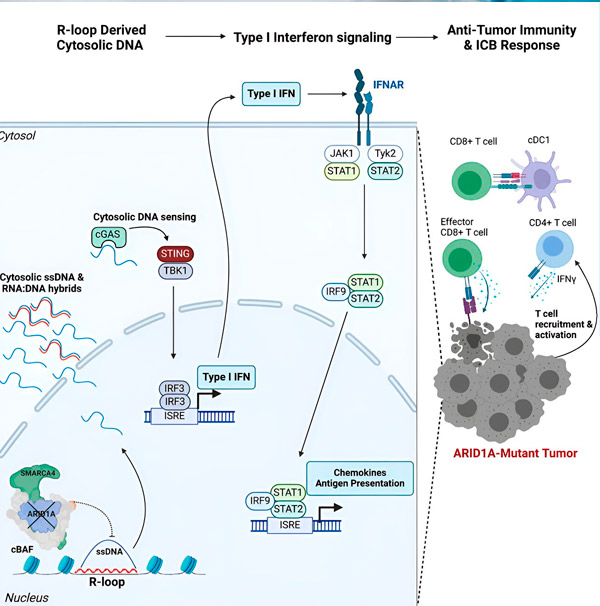
ที่มา: เซลล์ (2024) DOI: 10.1016/j.cell.2024.04.025
ทีมวิจัยได้สังเกตเห็นการตอบสนองภูมิคุ้มกันที่แข็งแกร่งในโมเดลทั้งหมดที่มีการกลายพันธุ์ของ ARID1A แต่ไม่เกิดขึ้นในโมเดลที่ ARID1A ทำงานได้ ซึ่งสนับสนุนแนวคิดที่ว่าการกลายพันธุ์ของ ARID1A เป็นตัวกระตุ้นการตอบสนองนี้ แต่สิ่งนี้ทำงานอย่างไรในระดับโมเลกุล?
แมทธิว แม็กซ์เวลล์ ผู้เขียนคนแรกของการศึกษานี้และนักศึกษาระดับบัณฑิตศึกษาในห้องปฏิบัติการฮาร์เกรฟส์ กล่าวว่า "เราพบว่า ARID1A มีบทบาทสำคัญในนิวเคลียสโดยรักษาการจัดระเบียบของดีเอ็นเอให้เหมาะสม หากไม่มี ARID1A ที่ทำงานได้ ดีเอ็นเออิสระจะถูกตัดออกและปล่อยสู่ไซโทซอล ทำให้เกิดการตอบสนองทางภูมิคุ้มกันต่อต้านไวรัสที่พึงประสงค์ ซึ่งสามารถเพิ่มขึ้นได้ด้วยการปิดกั้นจุดตรวจภูมิคุ้มกัน"
ยีน ARID1A เข้ารหัสโปรตีนที่ช่วยควบคุมรูปร่างของ DNA ของเราและรักษาเสถียรภาพของจีโนม เมื่อ ARID1A กลายพันธุ์ ก็จะกระตุ้นให้เกิดเหตุการณ์แบบเดียวกับ Rube Goldberg ในเซลล์มะเร็ง
ประการแรก การขาด ARID1A ที่ทำงานได้ผลทำให้มีการปล่อย DNA เข้าไปในไซโทซอล จากนั้น DNA ในไซโทซอลจะกระตุ้นระบบเตือนภัยต่อต้านไวรัสที่เรียกว่าเส้นทาง cGAS-STING เนื่องจากเซลล์ของเราได้รับการปรับให้ทำเครื่องหมาย DNA ใดๆ ในไซโทซอลว่าเป็นสิ่งแปลกปลอมเพื่อป้องกันการติดเชื้อไวรัส ในที่สุด เส้นทาง cGAS-STING จะกระตุ้นระบบภูมิคุ้มกันเพื่อดึงดูดเซลล์ T เข้าไปในเนื้องอกและกระตุ้นให้เซลล์เหล่านี้กลายเป็นเซลล์ T สังหารมะเร็งโดยเฉพาะ
ในแต่ละขั้นตอน ซึ่งขึ้นอยู่กับขั้นตอนก่อนหน้า ห่วงโซ่เหตุการณ์เหล่านี้ ได้แก่ การกลายพันธุ์ของ ARID1A การหลบหนีของ DNA สัญญาณเตือน cGAS-STING การคัดเลือกเซลล์ T ส่งผลให้จำนวนเซลล์ T ที่ต่อสู้กับมะเร็งในเนื้องอกเพิ่มขึ้น การปิดกั้นจุดตรวจภูมิคุ้มกันสามารถใช้เพื่อให้แน่ใจว่าเซลล์ T เหล่านี้ยังคงทำงานอยู่ ซึ่งจะช่วยเพิ่มความสามารถในการเอาชนะมะเร็ง
“ผลการค้นพบของเราให้กลไกโมเลกุลใหม่ซึ่งการกลายพันธุ์ของ ARID1A อาจมีส่วนสนับสนุนการตอบสนองทางภูมิคุ้มกันต่อเนื้องอก” ฮาร์เกรฟส์กล่าว “สิ่งที่น่าตื่นเต้นเกี่ยวกับผลการค้นพบเหล่านี้คือศักยภาพในการแปลผล เราสามารถใช้การกลายพันธุ์ของ ARID1A เพื่อคัดเลือกผู้ป่วยสำหรับการปิดกั้นจุดตรวจภูมิคุ้มกัน และตอนนี้เราพบกลไกที่ยาที่ยับยั้ง ARID1A หรือโปรตีนคอมเพล็กซ์ของมันอาจใช้เพื่อเสริมภูมิคุ้มกันบำบัดในผู้ป่วยรายอื่นๆ ต่อไป”
นักวิจัยได้อธิบายกลไกที่การปิดกั้นจุดตรวจภูมิคุ้มกันมีประสิทธิภาพมากขึ้นในมะเร็งที่มีการกลายพันธุ์ของ ARID1A ให้กับแพทย์ทราบถึงเหตุผลในการให้ความสำคัญกับภูมิคุ้มกันบำบัดนี้สำหรับผู้ป่วยที่มีการกลายพันธุ์ของ ARID1A ผลการวิจัยดังกล่าวถือเป็นก้าวสำคัญในการปรับการรักษามะเร็งให้เหมาะกับแต่ละบุคคล และเป็นแรงบันดาลใจในการพัฒนาวิธีการรักษาใหม่ๆ ที่มุ่งเป้าไปที่ ARID1A และโปรตีนคอมเพล็กซ์ของมัน
ในอนาคต ทีมสถาบัน Salk หวังว่าผลการค้นพบของพวกเขาจะช่วยปรับปรุงผลลัพธ์การรักษาสำหรับผู้ป่วยมะเร็งหลายประเภทที่เกี่ยวข้องกับการกลายพันธุ์ ARID1A และตั้งใจที่จะสำรวจการนำผลการวิจัยทางคลินิกนี้ไปปรับใช้ร่วมกับมหาวิทยาลัยแคลิฟอร์เนีย ซานดิเอโก
