สิ่งตีพิมพ์ใหม่
ยา LM11A-31 ช่วยชะลอการดำเนินของโรคอัลไซเมอร์ในการทดลอง
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter

ในการศึกษาวิจัยล่าสุดที่ตีพิมพ์ในวารสาร Nature Medicineนักวิทยาศาสตร์ได้ทำการศึกษาวิจัยแบบสุ่ม สองทางปกปิด และควบคุมด้วยยาหลอกในระยะ 2a เพื่อตรวจสอบความปลอดภัยและประสิทธิภาพของ LM11A-31 ในการรักษาโรคอัลไซเมอร์ (AD) ผ่านการปรับตัวรับ p75 neurotrophin (p75NTR)
โรคอัลไซเมอร์ระยะท้ายเป็นโรคสมองเสื่อมที่พบได้บ่อยที่สุด โดยมีลักษณะเด่นคือซินแนปส์ล้มเหลว เสื่อม และสูญเสียเซลล์ประสาท แม้ว่ายาทั้งสองชนิดที่ใช้รักษาโรคอัลไซเมอร์จะมุ่งเป้าไปที่การสะสมของโปรตีนอะไมลอยด์-β หรือโปรตีนเทาที่ผิดปกติ แต่ยาทั้งสองชนิดจะมุ่งเป้าไปที่พยาธิสรีรวิทยาเพียงบางส่วนเท่านั้น อีกวิธีหนึ่งคือการมุ่งเป้าไปที่ตัวรับและเครือข่ายสัญญาณที่มีอิทธิพลต่อเส้นทางชีวภาพพื้นฐาน การศึกษาก่อนทางคลินิกแสดงให้เห็นว่าการปรับ p75NTR ด้วยโมเลกุลเคมีขนาดเล็กชนิดใหม่ LM11A-31 จะช่วยลดการสูญเสียซินแนปส์ที่เกิดจากโปรตีนอะไมลอยด์และโปรตีนเทาที่ผิดปกติ
คำอธิบายการศึกษา
ในการทดลองทางคลินิกแบบสุ่มครั้งนี้ นักวิจัยตรวจสอบว่า LM11A-31 สามารถชะลอความก้าวหน้าของโรคอัลไซเมอร์โดยการปรับเปลี่ยน p75NTR ในมนุษย์ได้หรือไม่
ผู้เข้าร่วมการศึกษาได้รับแคปซูล LM11A-31 ช่องปากในขนาด 200 มก. และ 400 มก. หรือยาหลอกในอัตราส่วน 1:1:1 แก่ผู้ป่วยโรคหอบหืดระดับอ่อนถึงปานกลางจำนวน 242 รายเป็นเวลา 26 สัปดาห์ ผู้เข้าร่วมได้รับการยืนยันทางชีววิทยาว่าเป็นโรคอัลไซเมอร์ (ระดับโปรตีนเบต้าอะไมลอยด์ 42 (Aβ42) ในน้ำไขสันหลังต่ำกว่า 550 นาโนกรัมต่อลิตร หรืออัตราส่วน Aβ42:β40 ต่ำกว่า 0.89) ที่ได้รับการวินิจฉัยตามเกณฑ์ของ McKhann โดยมีคะแนน Mini-Psychiatric Examination (MMSE) 18 ถึง 26 คะแนน Geriatric Depression Scale (GDS) ต่ำกว่า 5.0 คะแนน Modified Hachinski Ischemic Scale (HIS) ≤ 4.0 การศึกษาอย่างเป็นทางการ ≥ 8 ปี และมีความเสื่อมถอยทางสติปัญญาก่อนหน้านี้ ≥ 6 เดือน
ผู้เข้าร่วมที่มีสิทธิ์ได้รับยาต้านอะเซทิลโคลีนเอสเทอเรส (AChEIs) หรือยาต้านตัวรับ NMDA บางส่วนเป็นเวลา ≥ 3 เดือนก่อนเข้าร่วมการศึกษา ผู้เข้าร่วมไม่ได้ใช้ยาผิดกฎหมาย เช่น ยารักษาโรคจิต เบนโซไดอะซีพีน ยาต้านโรคลมบ้าหมู ยากล่อมประสาท ยาลดความดันโลหิตที่ออกฤทธิ์ต่อระบบประสาทส่วนกลาง ยาเสริมสมอง (ยกเว้นแปะก๊วย) หรือยาแก้ปวดที่มีสารโอปิออยด์
ผลลัพธ์หลักของการศึกษาคือความปลอดภัยและการยอมรับ ซึ่งประเมินโดยใช้ Columbia Suicidal Thoughts and Behavior Severity Rating Scale (C-SSRS) สัญญาณชีพ ความดันโลหิต และพารามิเตอร์ทางโลหิตวิทยา การถ่ายภาพด้วยคลื่นแม่เหล็กไฟฟ้าโครงสร้าง (cMRI) การถ่ายภาพด้วยเครื่องเอกซเรย์ด้วยการปล่อยโพซิตรอนฟลูออโรดีออกซีกลูโคส (FDG-PET) และไบโอมาร์กเกอร์ของน้ำไขสันหลัง (CSF) ถูกนำมาใช้เพื่อประเมินผลลัพธ์ทางปัญญารอง การวัด AD ได้แก่ โปรตีน tau ที่ถูกฟอสโฟรีเลตโดย Thr181, โปรตีน tau ทั้งหมด, Aβ40, Aβ42 และกิจกรรมของ AChE ทีมใช้การทดสอบทางจิตวิทยาที่ปรับแต่งตามความต้องการเพื่อประเมินผลลัพธ์ทางปัญญารองในช่วงเริ่มต้น สัปดาห์ที่ 12 และ 26
ผลงานวิจัย
การศึกษาพบว่า LM11A-31 มีความปลอดภัยและเป็นที่ยอมรับได้ดี โดยไม่มีข้อกังวลด้านความปลอดภัยที่สำคัญ อาการไม่พึงประสงค์ที่พบบ่อยที่สุด ได้แก่ อาการปวดศีรษะ ท้องเสีย อีโอซิโนฟิเลีย และโพรงจมูกอักเสบ โดยปัญหาทางเดินอาหารและอีโอซิโนฟิเลียเป็นสาเหตุหลักของการหยุดใช้ยา มีผู้หยุดใช้ยาในกลุ่มยา 400 มก. มากกว่ากลุ่มยา 200 มก. และกลุ่มยาหลอก การตรวจ MRI ไม่พบข้อกังวลด้านความปลอดภัย รวมถึงความผิดปกติที่เกี่ยวข้องกับอะไมลอยด์ ไม่มีข้อแตกต่างที่สำคัญในคะแนนทางปัญญาหรือความผิดปกติของอะไมลอยด์ระหว่างกลุ่มการรักษาทั้งสองกลุ่ม
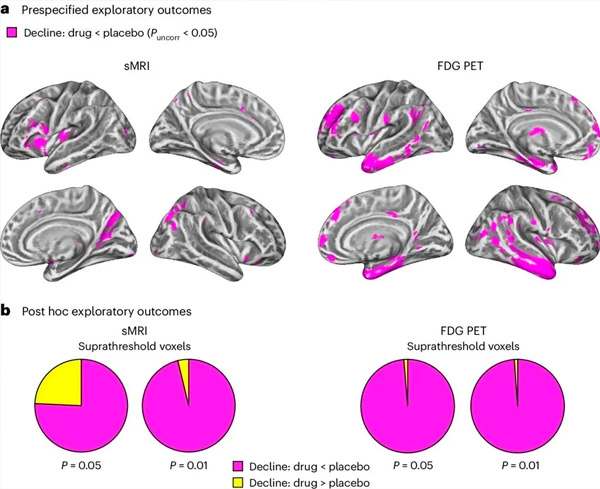
การวิเคราะห์ความแปรปรวนร่วมแบบสองทางโดยใช้แบบจำลองผสมสองทางได้ตรวจสอบปฏิสัมพันธ์ระหว่างการรักษา (ยาหรือยาหลอก) และเวลา (ก่อนหรือหลังการรักษา) คอนทราสต์แบบหางเดียวที่ตรวจสอบสมมติฐานปฏิสัมพันธ์ (ยาทำให้การดำเนินโรคช้าลงเมื่อเทียบกับยาหลอก) แสดงให้เห็นว่าการรักษาด้วย LM11A-31 ทำให้การเสื่อมตามยาวช้าลง (แผงด้านซ้าย) และการเผาผลาญกลูโคสต่ำลง (แผงด้านขวา) ในกลุ่มยา (cMRI, n = 127; PET, n = 121) เมื่อเปรียบเทียบกับกลุ่มยาหลอก (cMRI, n = 66; PET, n = 62) วอกเซลที่แสดงปฏิสัมพันธ์นี้จะแสดงที่เกณฑ์ที่ไม่ได้รับการแก้ไขที่ P < 0.05 (สีแดงอมม่วง) บนพื้นผิวคอร์เทกซ์เฉพาะประชากร ซีกซ้ายและซีกขวาจะแสดงในแถวบนและแถวล่างตามลำดับ บริเวณสมองที่แสดงปฏิสัมพันธ์ที่ไม่สอดคล้องกับสมมติฐานจะแสดงในรูปที่ 7 ในข้อมูลเสริม
B. จำนวนวอกเซลทั้งหมดในบริเวณสมองที่เสี่ยงต่อโรค AD ที่กำหนดไว้ล่วงหน้า (พื้นที่ทั้งหมดของแผนภูมิวงกลม) แสดงให้เห็นปฏิสัมพันธ์ที่สอดคล้องกับสมมติฐาน (สีแดงอมม่วง) หรือปฏิสัมพันธ์ที่ไม่สอดคล้องกับสมมติฐาน (สีเหลือง) ในแต่ละรูปแบบการถ่ายภาพ (cMRI แผงซ้าย; FDG PET แผงขวา) ที่เกณฑ์ที่เพิ่มขึ้นเรื่อยๆ ของ P < 0.01 และ P < 0.05 ที่ไม่ได้แก้ไข การจำลองแบบมอนติคาร์โลแสดงให้เห็นว่าอัตราส่วนของวอกเซลที่แสดงผลที่สอดคล้องกับสมมติฐานเทียบกับที่ไม่สอดคล้องกับสมมติฐานนั้นสูงกว่าอย่างมีนัยสำคัญเมื่อเทียบกับที่สังเกตได้จากข้อมูลที่สร้างแบบสุ่มสำหรับทั้ง cMRI และ PET (P < 0.001 สำหรับแต่ละรูปแบบ; การทดสอบสองหาง)
LM11A-31 ลดการเพิ่มขึ้นของ CSF Aβ42 และ Aβ40 ได้อย่างมีประสิทธิภาพเมื่อเทียบกับกลุ่มยาหลอก ยาตัวนี้ยังแสดงให้เห็นการลดลงของค่ามัธยฐานของการเปลี่ยนแปลงร้อยละต่อปีในไบโอมาร์กเกอร์โปรตีนก่อนไซแนปส์ SNAP25 และการลดลงของไบโอมาร์กเกอร์หลังไซแนปส์ NG ซึ่งบ่งชี้ถึงการชะลอตัวของการสูญเสียการเชื่อมต่อก่อนไซแนปส์และหลังไซแนปส์ LM11A-31 ยังลดการเพิ่มขึ้นของ YKL40 ส่งผลให้คะแนน MMSE ลดลงและคะแนน ADAS-Cog-13 เพิ่มขึ้น ยาตัวนี้ยังลดการสูญเสียเนื้อเทาในกลีบหน้าผากและคอร์เทกซ์พาริเอทัลส่วนหลัง และการลดลงของการเผาผลาญกลูโคสในบริเวณต่างๆ เช่น คอร์เทกซ์เอ็นโทไรนัล คอร์เทกซ์ขมับ ฮิปโปแคมปัส คอร์เทกซ์อินซูลาร์ และคอร์เทกซ์พรีฟรอนทัลอีกด้วย
บทสรุป
การศึกษาสรุปว่าการปรับ p75NTR โดย LM11A-31 นั้นเหมาะสำหรับการทดลองทางคลินิกขนาดใหญ่ LM11A-31 บรรลุจุดสิ้นสุดด้านความปลอดภัยหลักและได้รับการยอมรับอย่างดีในผู้ป่วย AD ระดับเบาถึงรุนแรง ผลลัพธ์บ่งชี้ถึงความจำเป็นในการศึกษาวิจัยเพิ่มเติมโดยใช้ระยะเวลาการรักษาที่นานขึ้นเพื่อประเมินศักยภาพของโมเลกุลขนาดเล็กในการควบคุม p75NTR ในฐานะการบำบัดเพื่อปรับเปลี่ยนโรคใน AD การศึกษาวิจัยแสดงให้เห็นว่า LM11A-31 ส่งผลต่อไบโอมาร์กเกอร์หลายตัวอย่างมีนัยสำคัญ รวมถึง Aβ40, Aβ42, SNAP25, NG และ YKL40 ซึ่งบ่งชี้ถึงการดำเนินของโรคที่ช้าลง การศึกษาวิจัยในอนาคตอาจประเมินตัวบ่งชี้สุขภาพของเซลล์เกลียเพิ่มเติม
