สิ่งตีพิมพ์ใหม่
การกระตุ้นภูมิคุ้มกันโดยกำเนิด: ส่วนสำคัญของกลไกที่ระบุ
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
นักวิจัยจาก LMU ได้ถอดรหัสปฏิสัมพันธ์ที่ซับซ้อนของเอนไซม์ต่างๆ รอบๆ ตัวรับภูมิคุ้มกันโดยกำเนิด Toll-like receptor 7 (TLR7) ซึ่งมีบทบาทสำคัญในการปกป้องร่างกายของเราจากไวรัส
ตัวรับ Toll-like 7 (TLR7) ซึ่งอยู่บนเซลล์เดนไดรต์ของระบบภูมิคุ้มกันของเรา มีบทบาทสำคัญในการป้องกันตามธรรมชาติของเราจากไวรัส TLR7 ตรวจจับไวรัสสายเดี่ยวและ RNA แปลกปลอมอื่นๆ และกระตุ้นการปล่อยตัวกลางการอักเสบ ความผิดปกติของตัวรับนี้ยังมีบทบาทสำคัญในโรคที่เกิดจากภูมิคุ้มกันทำลายตนเอง ทำให้การทำความเข้าใจและในอุดมคติ การปรับเปลี่ยนกลไกการทำงานของการทำงานของ TLR7 มีความสำคัญมากยิ่งขึ้น
นักวิจัยซึ่งนำโดยศาสตราจารย์ Veit Hornung และ Marlene Berouti จากศูนย์พันธุศาสตร์มิวนิกและภาควิชาชีวเคมีที่ LMU สามารถเจาะลึกกลไกการกระตุ้นที่ซับซ้อนได้มากขึ้น จากการศึกษาก่อนหน้านี้ ทราบกันดีว่าจำเป็นต้องตัดโมเลกุล RNA ที่ซับซ้อนเพื่อให้ตัวรับสามารถจดจำโมเลกุลเหล่านี้ได้
นักวิจัยของมหาวิทยาลัยแห่งรัฐมิสซูรีได้ค้นพบวิธีการประมวลผล RNA แปลกปลอมแบบสายเดี่ยวเพื่อตรวจจับ TLR7 โดยใช้เทคโนโลยีต่างๆ ตั้งแต่ชีววิทยาเซลล์ไปจนถึงกล้องจุลทรรศน์อิเล็กตรอนแบบแช่แข็ง ผลงานของพวกเขาได้รับการตีพิมพ์ในวารสาร Immunity
เอนไซม์หลายชนิดมีส่วนเกี่ยวข้องในการรับรู้ RNA จากภายนอก
ในช่วงวิวัฒนาการ ระบบภูมิคุ้มกันจะจำเพาะเจาะจงมากขึ้นในการตรวจจับเชื้อโรคจากสารพันธุกรรม ตัวอย่างเช่น ตัวรับภูมิคุ้มกันโดยกำเนิด TLR7 จะถูกกระตุ้นโดย RNA ของไวรัส เราสามารถมอง RNA ของไวรัสว่าเป็นสายโมเลกุลยาวๆ ที่มีขนาดใหญ่เกินกว่าจะจดจำได้ว่าเป็นลิแกนด์ของ TLR7 ซึ่งตรงนี้เองที่นิวคลีเอสเข้ามามีบทบาท เครื่องมือตัดโมเลกุลที่ตัด "สาย RNA" ออกเป็นชิ้นเล็กๆ
เอ็นโดนิวคลีเอสจะตัดโมเลกุล RNA ตรงกลางเหมือนกรรไกร ในขณะที่เอ็กโซนิวคลีเอสจะแยกสายจากปลายด้านหนึ่งไปยังอีกด้านหนึ่ง กระบวนการนี้จะสร้างชิ้นส่วน RNA ที่แตกต่างกันซึ่งสามารถจับกับช่องที่แตกต่างกันสองช่องบนตัวรับ TLR7 ได้ เฉพาะเมื่อช่องจับทั้งสองช่องบนตัวรับถูกชิ้นส่วน RNA เหล่านี้ครอบครองเท่านั้น จึงจะเกิดการส่งสัญญาณแบบคาสเคดที่กระตุ้นเซลล์และทำให้เกิดสถานะแจ้งเตือน
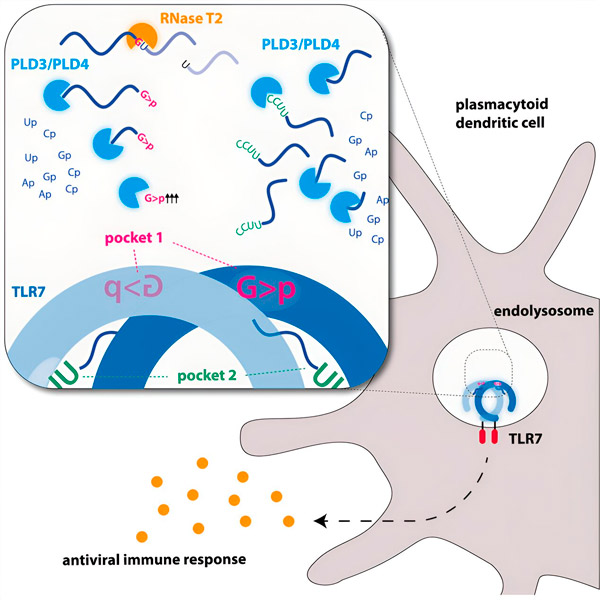
ภาพกราฟิก แหล่งที่มา: Immunity (2024). DOI: 10.1016/j.immuni.2024.04.010
นักวิจัยพบว่าการจดจำ RNA ของ TLR7 ต้องใช้กิจกรรมของเอ็นโดนิวคลีเอส RNase T2 ซึ่งทำงานร่วมกับเอ็กโซนิวคลีเอส PLD3 และ PLD4 (ฟอสโฟไลเปส D3 และ D4) ฮอร์นุงกล่าวว่า "แม้ว่าจะทราบกันดีว่าเอนไซม์เหล่านี้สามารถย่อยสลาย RNA ได้ แต่ตอนนี้เราได้แสดงให้เห็นแล้วว่าเอนไซม์เหล่านี้ทำปฏิกิริยากับ TLR7 และกระตุ้น TLR7"
การสร้างสมดุลของระบบภูมิคุ้มกัน
นักวิจัยยังพบอีกว่าเอ็กโซนิวคลีเอส PLD มีบทบาทสองประการในเซลล์ภูมิคุ้มกัน ในกรณีของ TLR7 เอ็กโซนิวคลีเอสมีฤทธิ์กระตุ้นการอักเสบ ในขณะที่ในกรณีของตัวรับ TLR อีกตัวหนึ่งคือ TLR9 เอ็กโซนิวคลีเอสมีฤทธิ์ต้านการอักเสบ “บทบาทสองประการของเอ็กโซนิวคลีเอส PLD นี้บ่งชี้ถึงความสมดุลที่ประสานกันอย่างดีในการควบคุมการตอบสนองภูมิคุ้มกันที่เหมาะสม” Berouti อธิบาย
“การกระตุ้นและยับยั้งการอักเสบพร้อมกันด้วยเอนไซม์เหล่านี้อาจทำหน้าที่เป็นกลไกป้องกันที่สำคัญเพื่อป้องกันความผิดปกติในระบบ” บทบาทของเอนไซม์อื่นๆ ในเส้นทางการส่งสัญญาณนี้และโมเลกุลที่เกี่ยวข้องเหมาะสมเป็นโครงสร้างเป้าหมายสำหรับการบำบัดหรือไม่ จะเป็นหัวข้อของการศึกษาวิจัยเพิ่มเติม
