สิ่งตีพิมพ์ใหม่
FDA อนุมัติการบำบัดใหม่สำหรับผู้ป่วยมะเร็งกาวเนื้อสมองเป็นครั้งแรกในรอบหลายทศวรรษ
ตรวจสอบล่าสุด: 02.07.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
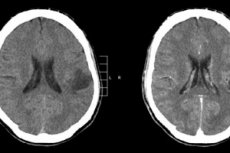
Vorasidenib ได้รับการรับรองจากสำนักงานคณะกรรมการอาหารและยาแห่งสหรัฐอเมริกา (FDA) สำหรับผู้ป่วยที่มีเนื้องอกในสมองเกรด 2 ที่มีการกลายพันธุ์ IDH1 หรือ IDH2
จากข้อมูลการทดลองทางคลินิกของ INDIGO ซึ่งเป็นการทดลองทางคลินิกแบบสุ่มสองทางปกปิดระยะ III ทั่วโลก พบว่า vorasidenib เพิ่มอัตราการรอดชีวิตโดยไม่มีการลุกลามของโรคได้มากกว่าสองเท่า และทำให้ความจำเป็นในการรักษาด้วยรังสีและเคมีบำบัดในผู้ป่วยมะเร็งกาวเนื้อสมองชนิดกลายพันธุ์ IDH เกรด 2 หลังการผ่าตัดตัดเนื้องอกล่าช้าลง INDIGO เป็นการทดลองทางคลินิกระยะ III ครั้งแรกของการบำบัดแบบกำหนดเป้าหมายสำหรับมะเร็งกาวเนื้อสมองชนิดกลายพันธุ์ IDH
“การศึกษาของ INDIGO แสดงให้เห็นว่าสารยับยั้ง IDH อาจใช้ได้ผลกับเนื้องอกในสมองระดับต่ำที่มีการกลายพันธุ์ของ IDH” ดร.แพทริก เวน ผู้อำนวยการศูนย์มะเร็งประสาทแห่งสถาบันมะเร็ง Dana-Farber และหนึ่งในประธานการศึกษากล่าว “ยาตัวสุดท้ายที่ได้รับการอนุมัติสำหรับเนื้องอกในสมองระดับต่ำได้รับการอนุมัติในปี 1999 ดังนั้นนี่จึงถือเป็นยาตัวใหม่ตัวแรกในรอบเวลานาน”
เนื้องอกในสมองเกรด 2 เป็นเนื้องอกในสมองที่รักษาไม่หาย การกลายพันธุ์ของ IDH พบได้ในเนื้องอกในสมองเกรดต่ำส่วนใหญ่
ประโยชน์สำคัญของการบำบัดด้วยวอราซิเดนิบคืออาจช่วยชะลอความจำเป็นในการฉายรังสีและเคมีบำบัดได้ การรักษาปัจจุบันประกอบด้วยการผ่าตัดตามด้วยการฉายรังสีและเคมีบำบัด การฉายรังสีและเคมีบำบัดเป็นการรักษาที่มีประสิทธิผล แต่หลังจากการรักษาเป็นเวลาหลายปี ผู้ป่วยจะเริ่มมีอาการผิดปกติทางสติปัญญา ซึ่งมักพบในผู้สูงอายุ
“ผู้ป่วยเหล่านี้มักมีอายุน้อย อยู่ในช่วงอายุ 30 หรือ 40 ปี แต่เมื่อเวลาผ่านไป 10 ถึง 20 ปี แม้ว่าเนื้องอกจะหายดีแล้ว แต่พวกเขามักมีอาการสมองเสื่อมหลังการฉายรังสีและเคมีบำบัด” เวินกล่าว “หากยาตัวนี้สามารถชะลอการเริ่มต้นการรักษาเหล่านี้ได้ ก็จะช่วยชะลอความผิดปกติของการรับรู้ในผู้ป่วยและรักษาคุณภาพชีวิตของพวกเขาไว้ได้”
การศึกษา INDIGO ครอบคลุมผู้ป่วย 331 รายที่มีเนื้องอกในสมองชนิดกลายพันธุ์ IDH เกรด 2 ซึ่งเข้ารับการผ่าตัดเพื่อนำเนื้องอกออก ผู้ป่วยที่เข้าร่วมการศึกษานี้ไม่จำเป็นต้องได้รับการฉายรังสีหรือเคมีบำบัดทันที และอยู่ในช่วงติดตามผล ในช่วงเวลาดังกล่าว ผู้ป่วยจะถูกสุ่มให้รับวอราซิเดนิบหรือยาหลอก
ผู้ป่วยที่รับวอราซิเดนิบมีอัตราการรอดชีวิตโดยไม่มีการลุกลามของโรคเฉลี่ยอยู่ที่ 27.7 เดือน เมื่อเทียบกับ 11.1 เดือนของผู้ป่วยที่รับยาหลอก เวลาในการเข้ารับการรักษาครั้งต่อไปของผู้ป่วยที่รับยาหลอกคือ 17.8 เดือน
ในผู้ป่วยที่ได้รับการรักษาด้วยวอราซิเดนิบ ค่ามัธยฐานไม่ได้ถูกกำหนด ณ เวลาของการวิเคราะห์ล่าสุด เนื่องจากจนถึงขณะนี้ มีเพียง 11.3% ของผู้ป่วยเหล่านี้เท่านั้นที่เปลี่ยนไปรับการรักษาครั้งต่อไป ยาตัวนี้ยังมีคุณสมบัติด้านความปลอดภัยที่จัดการได้
เวินกล่าวว่า “การศึกษานี้ไม่พบความแตกต่างในคุณภาพชีวิตเมื่อเทียบกับยาหลอก การยอมรับได้เป็นสิ่งสำคัญ เพราะเราคาดว่าผู้คนจะต้องใช้ยานี้เป็นเวลาหลายปี”
การอนุมัติดังกล่าวเปิดโอกาสให้ผู้ป่วยมีตัวเลือกใหม่ๆ หลายประการ ตัวอย่างเช่น วานกำลังศึกษาวิจัยการใช้โวราซิเดนิบร่วมกับภูมิคุ้มกันบำบัด และมีแผนศึกษาวิจัยการใช้โวราซิเดนิบร่วมกับการฉายรังสีและเคมีบำบัดมาตรฐาน
