สิ่งตีพิมพ์ใหม่
AI ตรวจพบมะเร็งต่อมลูกหมากระยะเริ่มต้นที่นักพยาธิวิทยาพลาด
ตรวจสอบล่าสุด: 23.08.2025

เนื้อหา iLive ทั้งหมดได้รับการตรวจสอบทางการแพทย์หรือตรวจสอบข้อเท็จจริงเพื่อให้แน่ใจว่ามีความถูกต้องตามจริงมากที่สุดเท่าที่จะเป็นไปได้
เรามีแนวทางการจัดหาที่เข้มงวดและมีการเชื่อมโยงไปยังเว็บไซต์สื่อที่มีชื่อเสียงสถาบันการวิจัยทางวิชาการและเมื่อใดก็ตามที่เป็นไปได้ โปรดทราบว่าตัวเลขในวงเล็บ ([1], [2], ฯลฯ ) เป็นลิงก์ที่คลิกได้เพื่อการศึกษาเหล่านี้
หากคุณรู้สึกว่าเนื้อหาใด ๆ ของเราไม่ถูกต้องล้าสมัยหรือมีข้อสงสัยอื่น ๆ โปรดเลือกแล้วกด Ctrl + Enter
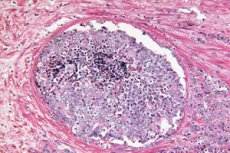
รายงานทางวิทยาศาสตร์แสดงให้เห็นว่าปัญญาประดิษฐ์สามารถตรวจจับสัญญาณทางสัณฐานวิทยาที่ซ่อนอยู่ของเนื้องอกในชิ้นเนื้อต่อมลูกหมาก ซึ่งก่อนหน้านี้นักพยาธิวิทยาเคยพิจารณาว่าไม่เป็นอันตราย แบบจำลองการเรียนรู้เชิงลึกที่ฝึกฝนโดยใช้วิธีการควบคุมแบบอ่อน (weakly supervised approach) สามารถทำนายได้ว่าผู้ชายที่มีค่า PSA สูงคนใดจะพัฒนาเป็นมะเร็งต่อมลูกหมากที่มีนัยสำคัญทางคลินิก (ISUP > 1) ในอีก 30 เดือนข้างหน้า และผู้ชายคนใดจะปราศจากมะเร็งอย่างน้อย 8 ปี วิธีนี้เปิดโอกาสให้มีการแบ่งกลุ่มความเสี่ยงตั้งแต่เนิ่นๆ ทันทีหลังจากการตัดชิ้นเนื้อ “สะอาด” ครั้งแรก และอาจช่วยตัดสินใจว่าใครกันแน่ที่จำเป็นต้องเข้ารับการผ่าตัดซ้ำและการเฝ้าระวังที่เข้มข้นยิ่งขึ้น
ความเป็นมาของการศึกษา
การเจาะชิ้นเนื้อต่อมลูกหมากด้วยเข็มปฐมภูมิมักให้ผลลบลวง กล่าวคือ มะเร็งที่มีนัยสำคัญทางคลินิกส่วนใหญ่ยังคง “อยู่นอกขอบเขต” โดยเฉพาะอย่างยิ่งเมื่อทำการตรวจชิ้นเนื้อแบบ TRUS แบบดั้งเดิม การนำระบบนำทางด้วย MRI มาใช้ทำให้สัดส่วนการตรวจพบมะเร็งที่มีนัยสำคัญทางคลินิกเพิ่มขึ้นและลดจำนวนการทำหัตถการซ้ำที่ไม่จำเป็น แต่แม้จะมีวิธีการที่ทันสมัย เนื้องอกที่ลุกลามบางชนิดก็ยังคงตรวจไม่พบ ปัญหาทางคลินิกยังคงเหมือนเดิม คือ ใครควรได้รับการตรวจติดตามหลังจากการตรวจชิ้นเนื้อแบบ “สะอาด” และใครควรได้รับการส่งตัวไปตรวจชิ้นเนื้อซ้ำตั้งแต่เนิ่นๆ เพื่อไม่ให้การวินิจฉัยล่าช้าและไม่ทำให้ผู้ป่วยต้องรับภาระหนักเกินไปจากการผ่าตัดแบบรุกราน
พื้นฐานทางชีววิทยาสำหรับการแก้ปัญหานี้คือปรากฏการณ์ TINT (tumor-instructed/indicating normal tissue) เนื้องอกจะ “ปรับเปลี่ยนโครงสร้าง” เนื้อเยื่อโดยรอบที่ดูเหมือนปกติของอวัยวะ ทิ้งร่องรอยที่อ่อนแอแต่เป็นระบบไว้ ตั้งแต่การปรับโครงสร้างของสโตรมาและภาวะพร่องออกซิเจนไปจนถึงการเปลี่ยนแปลงของเมตาบอลิซึม การเปลี่ยนแปลงเหล่านี้ได้รับการอธิบายไว้ในแบบจำลองการทดลองและในผู้ป่วยมะเร็งต่อมลูกหมาก และมีความสัมพันธ์กับความรุนแรงของเนื้องอก ซึ่งทำให้เนื้อเยื่อ “ปกติ” เป็นแหล่งสัญญาณการวินิจฉัยที่มีศักยภาพ แม้ว่าจะไม่มีต่อมมะเร็งที่เห็นได้ชัดในเนื้อเยื่อที่ตัดชิ้นเนื้อ
พยาธิวิทยาดิจิทัลและวิธีการเรียนรู้เชิงลึกมีเป้าหมายเพื่อดึงเอาลักษณะเฉพาะของสนามที่ “ละเอียดอ่อน” ดังกล่าวออกจากส่วน H&E มาตรฐาน ซึ่งแตกต่างจากสัณฐานวิทยาแบบคลาสสิกที่เน้นโครงสร้างของเนื้องอกที่เห็นได้ชัด อัลกอริทึมสามารถจับภาพรูปแบบที่กระจายตัวในสโตรมาและเยื่อบุผิวที่เกี่ยวข้องกับการมีอยู่ของเนื้องอกในส่วนอื่นของอวัยวะได้ วิธีนี้เปิดทางให้เกิดการแบ่งชั้นความเสี่ยงทันทีหลังจากผลการตรวจชิ้นเนื้อเป็นลบ: “คะแนน” ของแก้วที่สูงบ่งชี้ว่าควรทำการตรวจชิ้นเนื้อซ้ำตั้งแต่เนิ่นๆ หรือการนำภาพ MRI มาใช้ ในขณะที่คะแนนที่ต่ำบ่งชี้ว่าควรสังเกตอย่างอ่อนโยนมากขึ้น
นี่คือแนวคิดเบื้องหลังการศึกษาใหม่ในวารสาร Scientific Reports: ผู้เขียนได้ทดสอบว่า AI สามารถทำนายมะเร็งต่อมลูกหมากที่มีนัยสำคัญทางคลินิกในอีก 30 เดือนข้างหน้าได้หรือไม่ โดยอาศัยข้อมูลทางสัณฐานวิทยาจากการตรวจชิ้นเนื้อ TINT งานวิจัยนี้ต่อยอดจากเอกสารพิมพ์ล่วงหน้าที่นำเสนอก่อนหน้านี้ และเป็นพื้นฐานสำหรับการนำไบโอมาร์กเกอร์ดิจิทัลแบบ “สนาม” มาใช้ในการกำหนดเส้นทางผู้ป่วยหลังจากการตรวจชิ้นเนื้อแบบ “สะอาด” ครั้งแรก
วิธีการทำ: การออกแบบ ข้อมูล อัลกอริทึม
ผู้เขียนได้รวบรวมกลุ่มตัวอย่างชาย 232 คน ที่มีค่า PSA สูง และผลการตรวจชิ้นเนื้อด้วยเข็มเบื้องต้นระบุว่า "ไม่ร้ายแรง" (หลังจากการควบคุมทางเทคนิคแล้ว ผู้ป่วย 213 คน และเนื้อเยื่อ 587 ชิ้น ได้ถูกนำมาวิเคราะห์ขั้นสุดท้าย การตัดชิ้นเนื้อในปี พ.ศ. 2540-2559 ที่เมืองอูเมอา ประเทศสวีเดน) ผู้ป่วยแต่ละรายได้รับการจับคู่กับคู่ "กระจก" ตามอายุ ปีที่ได้รับการวินิจฉัย และระดับ PSA โดยครึ่งหนึ่งได้รับการวินิจฉัยว่าเป็นมะเร็งต่อมลูกหมากในภายหลัง (≤30 เดือน) และอีกครึ่งหนึ่งไม่มีมะเร็งเป็นเวลาอย่างน้อย 8 ปี สไลด์ H&E ถูกแปลงเป็นดิจิทัล (20 เท่า) ตัดเป็นไทล์พิกเซลขนาด 256×256 แล้วส่งไปยัง CLAM (Clustering-constrained Attention Multiple-Instance Learning) ซึ่งเป็นระบบการเรียนรู้แบบมีผู้ดูแลแบบอ่อนที่ทันสมัย โดยทราบเพียงชะตากรรมของผู้ป่วยเท่านั้น และไม่ทราบการทำเครื่องหมายของแต่ละพิกเซล คุณลักษณะต่างๆ ถูกสกัดโดย ResNet18 ซึ่งผ่านการฝึกอบรมล่วงหน้าจากชุดข้อมูลทางจุลพยาธิวิทยา 57 ชุด จุดสิ้นสุดคือไบนารี: ความเสี่ยงต่ำ (ไม่ร้ายแรง/ISUP1) เทียบกับความเสี่ยงสูง (ISUP2-5)
ความแม่นยำในการทำนาย
ในการทดสอบอิสระ แบบจำลองนี้มีค่า AUC เท่ากับ 0.81 ทั่วทั้งสไลด์ และมีค่า AUC เท่ากับ 0.82 ในระดับผู้ป่วย เมื่อถึงเกณฑ์ที่สมดุลและยอมรับได้ ความไวจะอยู่ที่ 0.92 โดยมีอัตราผลบวกลวงที่ 0.32 (ในระดับผู้ป่วย) กล่าวอีกนัยหนึ่ง ในกลุ่มคนที่ผลการตรวจชิ้นเนื้อครั้งแรก "ผิดพลาด" ระบบ AI สามารถระบุผู้ที่ได้รับการยืนยันว่าเป็นมะเร็งที่มีนัยสำคัญทางคลินิกได้ถูกต้อง แม้ว่าจะต้องแลกมาด้วยสัญญาณเตือนภัยลวงบางส่วนก็ตาม สำหรับคลินิก นี่คือสัญญาณว่า การตอบสนองของการตรวจชิ้นเนื้อ "ที่ไม่ร้ายแรง" ≠ ความเสี่ยงเป็นศูนย์ และสามารถแบ่งกลุ่มเชิงปริมาณได้ด้วยกระจกดิจิทัล
AI “สังเกต” อะไรในเนื้อเยื่อ “ปกติ” จริงๆ?
การตีความผ่าน UMAP และแผนที่ความสนใจแสดงให้เห็นว่าการเปลี่ยนแปลงของเนื้อเยื่อเกี่ยวพันมีข้อมูลมากที่สุด:
- คอลลาเจนในสโตรมาเพิ่มมากขึ้น (การอัดตัวของเมทริกซ์ “พังผืด”)
- เซลล์กล้ามเนื้อเรียบรอบต่อมมีจำนวนน้อยลง
- สัญญาณที่ละเอียดอ่อนในเยื่อบุผิวต่อมพบได้น้อยกว่า ซึ่งน่าจะต่ำกว่าความละเอียดในการดาวน์แซมปลิงที่มีอยู่
รูปแบบนี้สอดคล้องกับแนวคิด TINT (tumour-instructed/indicating normal tissue) ที่ว่า แม้แต่ "บรรทัดฐาน" ในอวัยวะที่เนื้องอกซ่อนอยู่ก็ถูกปรับเปลี่ยนโครงสร้างใหม่ภายใต้อิทธิพลของเนื้องอก และแตกต่างจาก "บรรทัดฐาน" ในอวัยวะที่ไม่มีเนื้องอก มะเร็งไม่ใช่แค่นิดัสเท่านั้น แต่ยังเป็นสนามแม่เหล็กด้วย และ AI เรียนรู้ที่จะอ่านผลของสนามแม่เหล็ก
แนวทางนี้มีประโยชน์ในทางปฏิบัติอย่างไร - สถานการณ์ที่อาจเกิดขึ้น
- การตรวจชิ้นเนื้อซ้ำตามความเสี่ยง: อัตรา AI ที่สูงบนกระจกที่ "สะอาด" - เหตุผลที่สนับสนุนการตรวจชิ้นเนื้อซ้ำในระยะเริ่มต้นหรือการนำทางด้วย MRI แทนที่จะรอ
- การปรับแต่งการตรวจติดตาม: ความเร็วต่ำช่วยชดเชยความวิตกกังวลหลังการตรวจ MRI แบบ "ไม่ชัดเจน" และช่วยควบคุมความเข้มข้นของการตรวจติดตามได้
- การฝึกรูปแบบ TINT: แผนที่ความสนใจและโอเวอร์เลย์แบบโต้ตอบช่วยให้นักพยาธิวิทยาสามารถมองเห็นฟิลด์ที่ละเอียดอ่อนรอบๆ มะเร็งได้ ซึ่งจะช่วยปรับปรุงความสอดคล้องของรายงาน
การเข้าใจข้อจำกัดเป็นสิ่งสำคัญ
ศูนย์แห่งนี้เป็นศูนย์เดียวในภาคเหนือของสวีเดน (ประชากรส่วนใหญ่เป็นชาวคอเคเชียน) การออกแบบเป็นแบบย้อนหลัง การตรวจชิ้นเนื้อพื้นฐานดำเนินการโดยไม่มีการนำทางด้วย MRI (การตรวจชิ้นเนื้อ TRUS อย่างเป็นระบบ) และเครื่องหมายบ่งชี้ผลลัพธ์ในอนาคต ไม่ใช่ "เนื้องอกแฝงบนสไลด์เดียวกัน" ยังไม่มีการตรวจสอบความถูกต้องจากภายนอกที่ศูนย์/เครื่องสแกนอิสระ และยังไม่มีการทดลองล่วงหน้าเกี่ยวกับผลกระทบของอัลกอริทึมต่อการตัดสินใจทางคลินิกและผลลัพธ์ อัตราผลบวกลวงยังคงมีนัยสำคัญ แบบจำลองนี้ไม่ได้แทนที่แพทย์ แต่เพิ่มชั้นความน่าจะเป็นสำหรับการตัดสินใจร่วมกัน
อะไรต่อไป: แผนงานการดำเนินการ
- การตรวจสอบภายนอกหลายศูนย์ (เครื่องสแกน โปรโตคอล กลุ่มชาติพันธุ์ที่แตกต่างกัน)
- การศึกษาการตัดสินใจล่วงหน้า: คะแนน AI เปลี่ยนแปลงวิถีการรักษาของผู้ป่วยหรือไม่ (เวลาในการวินิจฉัย จำนวนการตรวจชิ้นเนื้อซ้ำที่ไม่จำเป็น การวินิจฉัยเกิน/ไม่เพียงพอ)
- การบูรณาการกับ MRI และคลินิก: โมเดลรวม (PSA, MRI PIRADS, ปัจจัยทางคลินิก + คะแนน TINT ตาม H&E)
- ขั้นตอนทางเทคนิค: การทำให้การแปลงเป็นดิจิทัลเป็นมาตรฐาน การควบคุมการเคลื่อนตัวของข้อมูล ความสามารถในการอธิบาย (การซ้อนทับความสนใจสำหรับกิจวัตรประจำวัน)
ที่มา: Chelebian E., Avenel C., Järemo H., Andersson P., Bergh A., Wählby C. และคณะการค้นพบเนื้องอกที่บ่งชี้ถึงการเปลี่ยนแปลงทางสัณฐานวิทยาในชิ้นเนื้อต่อมลูกหมากชนิดไม่ร้ายด้วย AIรายงานทางวิทยาศาสตร์ (Nature Portfolio) เผยแพร่เมื่อวันที่ 21 สิงหาคม 2568 DOI: https://doi.org/10.1038/s41598-025-15105-6
